��Ŀ����
7������ˮ�е�NO${\;}_{3}^{-}$�����ཡ�������Σ����Ϊ�˽�������ˮ��NO${\;}_{3}^{-}$��Ũ�ȣ�ij��ȤС������������ַ�����a�������������£���Fe��OH��2��ԭNO${\;}_{3}^{-}$����ԭ����ΪNH3��
b���ڼ��������£������ۻ�ԭNO${\;}_{3}^{-}$����ԭ����ΪN2��
��1������a�У�����34g NH3��ͬʱ����16mol Fe��OH��3��
��2������b�з����ķ�Ӧ���£���ƽ�÷�Ӧ���ӷ���ʽ����
10Al+6NO${\;}_{3}^{-}$+4OH-�T10AlO${\;}_{2}^{-}$+3N2��+2H2O
��3������b�У�����0.15mol����ת��ʱ�����ɵĵ����ڱ�״���µ����Ϊ336mL��
���� ��1������n=$\frac{m}{M}$����17gNH3�����ʵ�������Ӧ��Fe��OH��2��Fe��OH��3��NO3-��NH3�����ݵ���ת�Ƽ�������Fe��OH��3�����ʵ�����
��2����Ӧ��Al��AlO2-��AlԪ�ػ��ϼ���0������Ϊ+3�ۣ�������3�ۣ�NO3-��N2������Ԫ�ػ��ϼ���+5�۽���Ϊ0�ۣ�������10�ۣ����ϼ�������С������Ϊ30����Al��ϵ��Ϊ10��N2ϵ��Ϊ3����ϵ���غ㡢ԭ���غ���ƽ�������ʵ�ϵ����
��3�����ݵ���ת���غ�������ɵ��������ʵ������ٸ���V=nVm���㵪���������
��� �⣺��1��34gNH3�����ʵ���Ϊ$\frac{34g}{17g/mol}$����Ӧ��Fe��OH��2��Fe��OH��3��NO3-��NH3�����ݵ���ת�ƿ�֪������Fe��OH��3�����ʵ���Ϊ$\frac{2mol��[5-��-3��]}{3-2}$=16mol��
�ʴ�Ϊ��16��
��2����Ӧ��Al��AlO2-��AlԪ�ػ��ϼ���0������Ϊ+3�ۣ�������3�ۣ�NO3-��N2������Ԫ�ػ��ϼ���+5�۽���Ϊ0�ۣ�������10�ۣ����ϼ�������С������Ϊ30����Al��ϵ��Ϊ10��N2ϵ��Ϊ3���ɵ�Ԫ���غ��֪ϵ��Ϊ6����AlԪ���غ��֪ϵ��Ϊ10���ɵ���غ��֪ϵ��Ϊ����HԪ���غ��֪ϵ��Ϊ������ƽ�����ӷ���ʽΪ��10Al+6NO3-+4OH-=10AlO2-+3N2��+2H2O��
�ʴ�Ϊ��10��6��4��10��3��2��
��3�����ݵ���ת���غ㣬��0.3mol����ת��ʱ���ɵ��������ʵ���Ϊ$\frac{0.15mol}{2��5}$=0.015mol�����������Ϊ0.015mol��22.4L/mol=0.336L=336mL���ʴ�Ϊ��336��
���� ���⿼��������ԭ��Ӧ����ƽ�����㡢��������ȣ���Ŀ�ѶȲ������ڿ���ѧ���Ի���֪ʶ���ۺ�Ӧ��������ע��Ի���֪ʶ���������գ�

| A�� | �÷�Һ©����Һʱ���ȴ����������²�Һ����ȫ�ֳ��ر��������ٴ��Ͽڵ����ϲ�Һ�� | |
| B�� | ȷ��ȡ25.00 mL��Һ���ѡ����Һ�ܡ���Ͳ��ζ��ܵ����� | |
| C�� | ���к��Ȳⶨʵ���У������NaOH��Һ��������m g����Ӧǰ����ϵ�¶ȱ仯����ӦҺ�ı�����Ϊc J•g-1•��-1��������1 molˮ�ų�������ΪkJ | |
| D�� | �ڳ���װ����ϴ�Ӿ���ʱ��Ϊ���پ����ܽ���ʧ��Ӧʹϴ�Ӽ�����ͨ����ֽ |
| A�� | Cu2+��Fe2+ | B�� | Cu2+��Fe3+ | C�� | Fe2+��Fe3+ | D�� | Fe2+��Cl- |
| A�� | a | B�� | 2a | C�� | 18a | D�� | 360a |
 ��úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú������
��úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú��������1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��C��s��+H2O��g��?CO��g��+H2��g����H=+131.3kJ/mol
�ٸ÷�Ӧ�ڸ��������Է����е�ԭ���ǡ�S��0
��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����BDF������ĸ����ͬ����
A�������е�ѹǿ���� B��1mol H-H �����ѵ�ͬʱ����2mol H-O ��
C��V ��CO��=V ��H2��D���ܱ��������ݻ����ٸı�
E������1mol ˮ��ͬʱ����1mol H2 F���������ܶȲ���
�۸÷�Ӧ��ƽ�ⳣ���ı���ʽK=$\frac{c��CO��•c��{H}_{2}��}{c��{H}_{2}O��}$��
��2��ˮú���ٽ�һ����Ӧ����ȡ��������ӦΪH2O��g��+CO��g��?H2��g��+CO2��g����ij��
���¸÷�Ӧ���淴Ӧƽ�ⳣ��K=$\frac{4}{9}$�����¶����ڼס��ҡ������������ܱ������У�ֻ
Ͷ��H2��g����CO2��g��������ʼŨ�����±���ʾ�������жϲ���ȷ����B��
| ��ʼ Ũ�� | �� | �� | �� |
| c��H2��/mol/L | 0.010 | 0.020 | 0.020 |
| c��CO2��/mol/L | 0.010 | 0.010 | 0.020 |
B��ƽ��ʱ�����кͱ���H2��ת���ʲ���
C��ƽ��ʱ������c��CO2���Ǽ��е�2 ��
D��ƽ��ʱ������CO2��ת���ʴ���60%
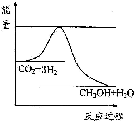
��3��Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g������ͼ��ʾ�÷�Ӧ���й�������������λΪkJ•mol-1���ı仯�������Ϊ1L �ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc ��CH3OH����С����A��
A�������¶� B������He��g����ʹ��ϵѹǿ����
C����H2O��g������ϵ�з������ D���ٳ���1mol CO2 ��3mol H2��
| A�� | ��ȩ | B�� | ����ȩ��ͬϵ�� | ||
| C�� | CH3CH2COCH3 ��2-��ͪ�� | D�� | CH2=C��CH3��CHO |
 ��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺
��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺ �������ճ������г��������ᣮ
�������ճ������г��������ᣮ