题目内容
20.下列属于电解质的是( )| A. | 氢氧化钠固体 | B. | 浓盐酸 | C. | 铜 | D. | 蔗糖 |
分析 在水溶液里或熔融状态下能导电的化合物是电解质,电解质首先必须是化合物,水溶液中和熔融状态下都不导电的化合物为非电解质,根据定义分析解答.
解答 解:A.氢氧化钠固体水溶液中完全电离出阴阳离子,溶液能导电,氢氧化钠为强电解质,故A正确;
B.浓盐酸溶液是氯化氢气体的水溶液为混合物,所以盐酸溶液不是电解质,故B错误;
C.铜为单质,既不是电解质也不属于非电解质,故C错误;
D.蔗糖的水溶液和熔融状态都不导电,所以蔗糖是非电解质,故D错误.
故选A.
点评 本题考查了电解质的判断,难度不大,注意电解质是指化合物,水溶液中或熔融状态下导电是判断依据,题目较简单.

练习册系列答案
相关题目
10.下列化学用语或模型表示正确的是( )
| A. | 硝基苯的结构简式: | B. | CO2分子比例模型: | ||
| C. | NH4Cl的电子式: | D. | NaCl的晶体模型: |
11.下列说法中正确的是( )
| A. | 金刚石、碳化硅、晶体硅的熔点依次升高 | |
| B. | CO2和SiO2 化学式相似,物理性质也相似 | |
| C. | CH3CH(CH2OH)CH2OOCCH3是一种手性分子,水解后手性消失 | |
| D. | 水加热到很高的温度都难以分解是因为水分子间存在氢键 |
8.通常人们把拆开 1mol 某化学键吸收的能量看成该化学键的键能.键能的大小可以衡量化 学键的强弱,也可以估计化学反应的反应热.下列是一些化学键的键能.
根据键能数据估算反应 CH4+4F2=CF4+4HF 每消耗 1mol CH4的热效应( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | 放热 1940 kJ | B. | 吸热 1940 kJ | C. | 放热 485 kJ | D. | 吸热 485 kJ |
5.下列说法正确的是( )
| A. | 金属钠投入氯化亚铁溶液可制取氢氧化铁胶体 | |
| B. | 镁带燃烧可以用二氧化碳灭火器扑灭 | |
| C. | 铁能从硫酸铜溶液中置换出铜,生成硫酸铁 | |
| D. | 硅酸的酸酐是二氧化硅,能溶于氢氟酸 |
12.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1molFeBr2与1molCl2反应时转移的电子数为1NA | |
| B. | 10g H218O与D216O的混合物中所含中子、电子数目均为5NA | |
| C. | 标况下,22.4L甲烷中含有C-H键数为1NA | |
| D. | pH=2的H2SO4溶液1L,含H+的数目为0.02NA |
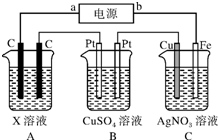 如图所示,电解一段时间后,测得C中Ag+减少了0.1mol,Fe电极被溶解.试回答:
如图所示,电解一段时间后,测得C中Ag+减少了0.1mol,Fe电极被溶解.试回答: