题目内容
10.某学习小组在对G、Q、X、Y、Z等五种均含氯的化合物的性质进行探究时发现,它们之间有如下转化关系:①G→Q+NaCl;
②Q+H2O-→X+H2;
③Y+NaOH→G+Q+H2O;④Z+NaOH→X+Q+H2O.
请根据该小组的探究结果,对这五种氯的化合物按氯元素化合价由低到高的顺序排列正确的是( )
| A. | GQXYZ | B. | XYGQZ | C. | GYQZX | D. | GXQYZ |
分析 G、Q、X、Y、Z均为氯的含氧化合物,根据氧化还原反应中Cl元素的化合价升降来分析,氧化还原反应中元素的化合价有升高,则必然有降低,以此来解答.
解答 解:①G→Q十NaCl中,NaCl中Cl元素为-1价,则Cl元素的化合价为Q>G>-1,
③Y十NaOH→G十Q十H2O中,结合①可知Cl元素的化合价为Q>Y>G,
②Q+H2O→X+H2中,H元素的化合价降低,则Cl元素的化合价升高,所以Cl元素的化合价为X>Q,
④Z十NaOH→Q十X十H2O中,结合②可知,Cl元素的化合价为X>Z>Q,
所以五种化合物中氯的化合价由低到高的顺序为GYQZX,
故选C.
点评 本题考查氧化还原反应,明确氧化还原反应中元素的化合价变化是解答本题的关键,题目难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
20.4.6g纯净金属钠在干燥空气中被氧化后,得到7.0g固体,由此可判断其氧化产物是( )
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O2和Na2O | D. | 无法确定 |
1.某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1-2滴溴水,振荡后溶液呈黄色.
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含Br2(填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致.
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.
供选用的试剂:a.酚酞试液;b.CCl4; c.无水酒精;d. KSCN溶液.
请你在下表中写出丙同学选用的试剂及实验中观察到的现象.(试剂填序号)
(4)结论
氧化性:Br2>Fe3+.故在足量的稀氯化亚铁溶液中,加入1-2滴溴水,溶液呈黄色所发生的离子反应方程式为2Fe2++Br2=2Fe3++2Br-.
(5)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是Fe2+(填离子的化学式).
②在100mL FeBr2溶液中通入2.24L Cl2(标准状况),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量的浓度为1mol/L.
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含Br2(填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致.
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.
供选用的试剂:a.酚酞试液;b.CCl4; c.无水酒精;d. KSCN溶液.
请你在下表中写出丙同学选用的试剂及实验中观察到的现象.(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案1 | ||
| 方案2 |
氧化性:Br2>Fe3+.故在足量的稀氯化亚铁溶液中,加入1-2滴溴水,溶液呈黄色所发生的离子反应方程式为2Fe2++Br2=2Fe3++2Br-.
(5)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是Fe2+(填离子的化学式).
②在100mL FeBr2溶液中通入2.24L Cl2(标准状况),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量的浓度为1mol/L.
5.已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S:Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是( )
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S:Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是( )
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuCO3<Cu(OH)2<CuS | C. | CuS<CuCO3<Cu(OH)2 | D. | Cu(OH)2<CuCO3<CuS |
2.下列实验装置能达到实验目的是( )
| A. | 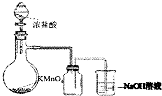 实验室制取并收集Cl2 | B. | 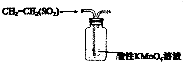 检验乙烯中是否含有SO2 | ||
| C. | 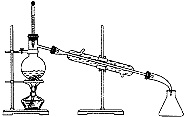 分离Br2和H20的混合物 | D. | 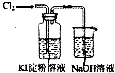 验证氧化性Cl>I2 |
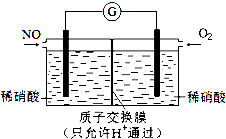 NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.
NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.