题目内容
20. 氟在自然界中常以CaF2的形式存在.
氟在自然界中常以CaF2的形式存在.(1)氟离子的外围电子排布式为2s22p6.HF能以任意比例溶于水,除了因为HF是极性分子外,还因为H2O与HF形成分子间氢键.
(2)F2通入稀NaOH溶液中可生成OF2,OF2分子中氧原子的杂化方式为sp3.
(3)下列有关CaF2的表达正确的是bd.
a.Ca2+与F-间仅存在静电吸引作用
b.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
c.阴阳离子比为2:1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
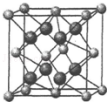
(4)CaF2晶胞结构如图,与一个Ca2+等距离且最近的Ca2+有12个.
(5)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是3CaF2+Al3+=3Ca2++AlF63- (用离子方程式表示)( 已知AlF63-在溶液中可稳定存在).
分析 (1)F的离子核有10个电子,分两层排布,最外层有8个电子;HF与水分子间能形成氢键;
(2)根据价层电子对互斥理论分析,先计算价层电子对数,再判断中心原子的杂化类型;
(3)a.阴阳离子间存在静电引力和静电斥力,则;
b.离子晶体的熔点与离子所带电荷、离子半径有关;
c.晶体的结构与电荷比、半径比有关;
d.离子化合物在熔融时能发生电离;
(4)根据CaF2晶胞结构,结合钙离子的位置判断;
(5)F-与Al3+能形成很难电离的配离子AlF63-.
解答 解:(1)氟离子核有10个电子,分两层排布,最外层有8个电子,则氟离子的外围电子排布式为2s22p6,H2O与HF形成分子间氢键,二者互溶;
故答案为:2s22p6;H2O与HF形成分子间氢键;
(2)OF2分子中O原子的价层电子对数=2+$\frac{1}{2}$(6-2×1)=4,则O原子的杂化类型为sp3杂化,
故答案为:sp3;
(3)a.阴阳离子间存在静电引力和静电斥力,Ca2+与F-间存在静电吸引作用,还存在静电斥力,故a错误;
b.离子晶体的熔点与离子所带电荷、离子半径有关,离子半径越小,离子晶体的熔点越高,所以CaF2的熔点高于CaCl2,故b正确;
c.晶体的结构与电荷比、半径比有关,阴阳离子比为2:1的物质,与CaF2晶体的电荷比相同,若半径比相差较大,则晶体构型不相同,故c错误;
d.CaF2中的化学键为离子键,离子化合物在熔融时能发生电离,存在自由移动的离子,能导电,因此CaF2在熔融状态下能导电,故b正确;
故答案为:bd;
(4)图中CaF2晶体在每个晶胞中与Ca2+离子最近且等距离的Ca2+离子数为3个,通过每个Ca2+可形成8个晶胞,每个Ca2+计算2次,所以与Ca2+离子最近且等距离的Ca2+离子数为(8×3)÷2=12个,
故答案为12;
(5)CaF2难溶于水,但可溶于含Al3+的溶液中,因为在溶液中F-与Al3+能形成很难电离的配离子AlF63-,使CaF2的溶解平衡正移,其反应的离子方程式为:3CaF2+Al3+=3Ca2++AlF63-;
故答案为:3CaF2+Al3+=3Ca2++AlF63-.
点评 本题考查了物质结构与性质,题目涉及离子的外围电子排布式、晶体熔沸点的比较、化学键、沉淀溶解平衡、杂化理论的应用等,题目涉及的知识点较多,侧重于考查学生对基础知识的综合应用能力,题目难度中等.

N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=-533.23kJ•mol-1
H2O(g)=H2O (l)△H2=-44kJ•mol-1
2H2O2(l)=2H2O(l)+O2(g)△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
| A. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
| A. | 制造普通水泥和玻璃的主要原料都用到石灰石 | |
| B. | 工业上制玻璃不会有温室气体的排放 | |
| C. | 玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料 | |
| D. | “中国”的英文单词叫China,这是由于中国制造的某种物质驰名世界,这种物质是陶瓷 |
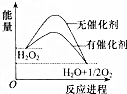 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2=H2O+O2;△H=-Q1 kJ•mol-1 | |
| D. | 加入催化剂,减小了反应的热效应 |
| A. | NH4+、NO3-、Na+、SO42- | B. | H+、Fe2+、Na+、NO3- | ||
| C. | Ba2+、K+、Al3+、HCO3- | D. | NH4+、Li+、OH-、SO42- |
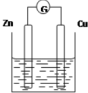 如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下: