题目内容
14.4gNaOH溶解在10mL水中,稀释至1L后,取出10mL其物质的量浓度是( )| A. | 0.1mol/L | B. | 1mol/L | C. | 0.01mol/L | D. | 10mol/L |
分析 根据n=$\frac{m}{M}$计算出4g氢氧化钠的物质的量,稀释过程中溶质的物质的量不变,再根据c=$\frac{n}{V}$计算出稀释后氢氧化钠溶液的浓度,最后根据溶液具有均一性判断取出的10mL溶液的浓度.
解答 解:4g氢氧化钠的物质的量为:$\frac{4g}{40g/mol}$=0.1mol,
稀释过程中氢氧化钠的物质的量不变,则稀释后溶液中氢氧化钠的浓度为:c=$\frac{0.1mol}{1L}$=0.1mol/L,
溶液具有均一性,则取出的10mL溶液的浓度不变,仍然为0.1mol/L,
故选 A.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意熟练掌握物质的量与摩尔质量、物质的量浓度的关系,试题培养了学生的化学计算能力.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
4.下列说法或表述中正确的是( )
| A. | 某有机化合物完全燃烧生成等物质的量的CO2和H2O,则该有机物的分子式一定CnH2n | |
| B. | 烷烃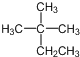 的系统命名为2-甲基-2-乙基丙烷 的系统命名为2-甲基-2-乙基丙烷 | |
| C. | 如图所示的有机物分子式为C14H12O2,能发生银镜反应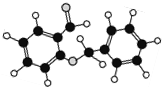 | |
| D. | 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH |
5.己烷雌酚的一种合成路线如图:

下列叙述不正确的是( )

下列叙述不正确的是( )
| A. | 用FeCl3溶液可以鉴别化合物X和Y | |
| B. | Y的苯环上的二氯取代物有8种同分异构体 | |
| C. | 在NaOH水溶液中加热,化合物X发生消去反应 | |
| D. | X转化为Y的反应类型为取代反应 |
2.下列物质中与其他三组不同的是( )
| A. | 金刚石、石墨、C60 | B. | 红磷、白磷 | ||
| C. | 一氧化碳、二氧化碳 | D. | 氧气、臭氧 |
9.下列化学用语正确的是( )
| A. | 乙烯分子的球棍模型: | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 乙炔的实验式:C2H2 | D. | 2-甲基-1,3-丁二烯的键线式: |
19.下列离子方程式书写错误的是( )
| A. | 在NaHSO4溶液中加Ba(OH)2至中性:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$=BaSO4↓+2H2O | |
| B. | 向硫酸铜溶液中通入H2S气体:Cu2++H2S═CuS↓+2H+ | |
| C. | SO2气体通入Ba(OH)2溶液中:SO2+2OH-═SO${\;}_{3}^{2-}$ | |
| D. | 用稀硫酸酸化硫化钠和亚硫酸钠的混合溶液:SO${\;}_{3}^{2-}$+2S2-+6H+═3S↓+3H2O |
6.下列离子方程式书写正确的是( )
| A. | 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 氧化镁与稀盐酸混合:O2-+2H+═2Cl--+H2O | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 盐酸与澄清石灰水反应:H++OH-═H2O |
3.为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是
( )
| 物质 | 试剂 | 分离方法 | |
| ① | 硝酸钾固体(氯化钠) | 蒸馏水 | 降温结晶 |
| ② | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| ③ | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| ④ | 氯气(氯化氢) | 饱和氯化钠溶液 | 洗气 |
| A. | ①③ | B. | ①④ | C. | 只有② | D. | ③④ |
4.在给定条件的水溶液中能大量共存的粒子组是( )
| A. | 无色透明的溶液中:Fe3+、K+、OH-、NO3- | |
| B. | 能使石蕊试剂变红的溶液:SO42-、Cl-、Cu2+、NH4+ | |
| C. | 强碱性溶液中:K+、Ca2+、Cl-、HCO3- | |
| D. | 强酸性溶液中:Na+、Fe2+、Cl-、ClO- |