题目内容
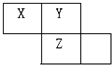 X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )| A、Z的氧化物对应的水化物一定是一种强酸 |
| B、原子半径大小顺序是X>Y>Z |
| C、Z单质与Fe反应形成的化合物中,铁元素显+3价 |
| D、Y的单质比Z的单质更易与氢气反应 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W均为短周期元素,根据它们在周期表中的位置知,X、Y是第二周期元素,Z为第三周期元素,Y和Z位于同一主族,Y原子的最外层电子数是次外层电子数的3倍,Y是O元素,则X是N元素、Z是S元素,
A.Z元素的氧化物对应的水化物有亚硫酸和硫酸;
B.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
C.Z单质具有弱氧化性,能将变价金属氧化为较低价态;
D.元素的非金属性越强,其单质与氢气反应越容易.
A.Z元素的氧化物对应的水化物有亚硫酸和硫酸;
B.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
C.Z单质具有弱氧化性,能将变价金属氧化为较低价态;
D.元素的非金属性越强,其单质与氢气反应越容易.
解答:
解:X、Y、Z、W均为短周期元素,根据它们在周期表中的位置知,X、Y是第二周期元素,Z为第三周期元素,Y和Z位于同一主族,Y原子的最外层电子数是次外层电子数的3倍,Y是O元素,则X是N元素、Z是S元素,
A.Z元素的氧化物对应的水化物有亚硫酸和硫酸,硫酸是强酸、亚硫酸是弱酸,故A错误;
B.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径大小顺序是Z>X>Y,故B错误;
C.Z是S元素,S单质具有弱氧化性,能将变价金属氧化为较低价态,所以Z单质与Fe反应形成的化合物中,铁元素显+2价,故C错误;
D.元素的非金属性越强,其单质与氢气反应越容易,非金属性Y>Z,所以Y的单质比Z的单质更易与氢气反应,故D正确;
故选D.
A.Z元素的氧化物对应的水化物有亚硫酸和硫酸,硫酸是强酸、亚硫酸是弱酸,故A错误;
B.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径大小顺序是Z>X>Y,故B错误;
C.Z是S元素,S单质具有弱氧化性,能将变价金属氧化为较低价态,所以Z单质与Fe反应形成的化合物中,铁元素显+2价,故C错误;
D.元素的非金属性越强,其单质与氢气反应越容易,非金属性Y>Z,所以Y的单质比Z的单质更易与氢气反应,故D正确;
故选D.
点评:本题考查元素周期表和元素周期律的综合应用,侧重考查分析、知识运用能力,明确同一周期、同一主族元素原子结构、元素性质递变规律是解本题关键,易错选项是A,题目难度不大.

练习册系列答案
相关题目
溶液A中加入一定量的NaF晶体后,若测得c(Na+)与c(F-)接近相等,则溶液A的pH值不可能为( )
| A、6 | B、7 | C、8 | D、9 |
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法正确的是( )


| A、充电时电极b连接电源的正极 |
| B、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| C、放电时正极的电极反应式为Zn-2e-═Zn2+ |
| D、充电时左侧电解质储罐中的离子总浓度增大 |
已知H-H键能为436KJ/mol,H-N键能为391kJ/mol,根据化学方程式:N2+3H2═2NH3 △H=-92.4kJ/mol,则N≡N键的键能是( )
| A、431 kJ/mol |
| B、945.6 kJ/mol |
| C、649 kJ/mol |
| D、869 kJ/mol |
下列物质中,既含有离子键,又含有共价键的是( )
| A、NaOH |
| B、Na2O |
| C、MgCl2 |
| D、H2O2 |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、33.6升CO2与O2的混合气中,含有的氧原子数为3 NA |
| B、15克甲基正离子(CH3+)含有的电子数为8NA |
| C、1molCl2与任何物质充分作用,转移电子数都为2NA |
| D、将0.1 mol N2和0.3 mol H2置于密闭容中充分反应,可得0.2NA个NH3分子 |
下列说法正确的是(NA为阿伏加德罗常数)( )
| A、电解精炼铜时,当阳极上质量减少6.4g时,电路上转移的电子数目为0.2 NA |
| B、1L 1.0mol?L-1NH4Cl与2L 0.5mol?L-1NH4HSO4溶液含NH4+数目相同 |
| C、0.2mol Zn与一定量浓H2SO4恰好完全反应,生成的气体分子数必为0.2NA |
| D、将2mL0.5 mol?Lˉ1Na2SiO3溶液滴入稀盐酸中制得H4 SiO4胶体,所含胶粒数为0.001NA |
下列有相关说法不正确的是( )
| A、某吸热反应能自发进行,因此该反应是熵增反应 |
| B、在任何条件下,纯水都呈中性 |
| C、水的离子积常数Kw随温度、外加酸(碱)浓度的改变而改变 |
| D、铅蓄电池充电时,标有“-”的电极应与电源的负极相连 |
已知某无色溶液中含有K+、Cl-、SO42-三种离子,则下列离子在该溶液中可能大量存在的是( )
| A、Ba2+ |
| B、Mg2+ |
| C、Ag+ |
| D、MnO42- |