题目内容
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、0.2mol?L-1 FeCl3溶液中含有Cl-总数为0.6NA |
| B、次氯酸光照分解产生22.4mL气体(标准状况下),转移电子数为0.002NA |
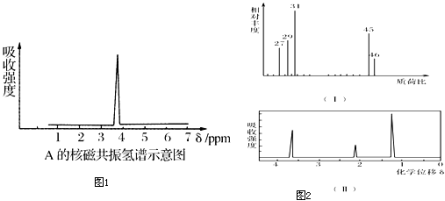
| C、常温下,4.6g乙醇含有C-H键总数为0.6NA |
| D、常温常压下,4.4g CO2和4.4g N2O的原子总数都是0.3NA |
考点:阿伏加德罗常数
专题:离子反应专题
分析:A.缺少氯化氢溶液的体积,无法计算溶液中氯离子的数目;
B.标况下22.4mL氧气的物质的量为0.001mol,根据2HClO
2HCl+O2↑可知,生成0.001mol氧气转移了0.004mol电子;
C.乙醇的结构式为: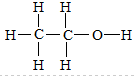 ,乙醇分子中含有5个碳氢键;
,乙醇分子中含有5个碳氢键;
D.
B.标况下22.4mL氧气的物质的量为0.001mol,根据2HClO
| ||
C.乙醇的结构式为:
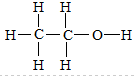 ,乙醇分子中含有5个碳氢键;
,乙醇分子中含有5个碳氢键;D.
解答:
解:A.由于溶液的体积未知,不能根据n=c?V求出氯化铁的物质的量,也不能求氯离子的物质的量,故A错误;
B.根据次氯酸的性质及化合价升降总数等于转移电子数可得:2HClO
2HCl+O2↑~4e-,则n(O2)=0.001mol,转移电子与氧气的系数之比等于物质的量之比,则每产生0.001mol氧气,次氯酸分解反应转移0.004mol电子,转移电子数为0.004NA,故B错误;
C.由于乙醇的相对分子质量为46,则4.6g乙醇的物质的量为:n(C2H5OH)=
=0.1mol,根据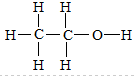 可知,1个乙醇分子中含有5个C-H键、1个C-C键、1个O-H键,则0.1mol乙醇含有0.5molC-H键,含有C-H键总数为0.5NA,故C错误;
可知,1个乙醇分子中含有5个C-H键、1个C-C键、1个O-H键,则0.1mol乙醇含有0.5molC-H键,含有C-H键总数为0.5NA,故C错误;
D.由于二氧化碳和一氧化二氮的相对分子质量都是44,则n(CO2)=0.1mol,n(N2O)=0.1mol,由于1个二氧化碳分子含有3个原子、1个一氧化二氮分子含有3个原子,则0.1mol二氧化碳分子含有0.3mol原子、0.1mol一氧化二氮分子含有0.3mol原子,二者含有的原子总数都是0.3NA,故D正确;
故选D.
B.根据次氯酸的性质及化合价升降总数等于转移电子数可得:2HClO
| ||
C.由于乙醇的相对分子质量为46,则4.6g乙醇的物质的量为:n(C2H5OH)=
| 4.6g |
| 46g/mol |
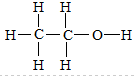 可知,1个乙醇分子中含有5个C-H键、1个C-C键、1个O-H键,则0.1mol乙醇含有0.5molC-H键,含有C-H键总数为0.5NA,故C错误;
可知,1个乙醇分子中含有5个C-H键、1个C-C键、1个O-H键,则0.1mol乙醇含有0.5molC-H键,含有C-H键总数为0.5NA,故C错误;D.由于二氧化碳和一氧化二氮的相对分子质量都是44,则n(CO2)=0.1mol,n(N2O)=0.1mol,由于1个二氧化碳分子含有3个原子、1个一氧化二氮分子含有3个原子,则0.1mol二氧化碳分子含有0.3mol原子、0.1mol一氧化二氮分子含有0.3mol原子,二者含有的原子总数都是0.3NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项A、C为易错点,注意A缺少溶液体积、C中乙醇分子含有5个碳氢键.

练习册系列答案
相关题目
中学化学中很多“规律”都可以类推,下列根据有关“规律”推出的结论正确的是( )
| A、CO2为直线形分子,故CS2也为直线形分子 |
| B、浓硫酸可以干燥HCl气体,故也可用浓硫酸干燥HI气体 |
| C、Na在空气中燃烧会生成Na2O2,故Li在空气中燃烧也会生成Li2O2 |
| D、卤族元素单质随核电荷数增加熔点升高,故碱金属单质熔点也随核电荷数增加而升高 |
M是一种常见的大气污染物,其在空气中的含量是环境空气质量的重要测评指标.该气体具有漂白性,能使品红溶液褪色,加热后溶液颜色又能恢复.M的化学式为( )
| A、SO2 |
| B、CO2 |
| C、HCl |
| D、NO |
下列叙述正确的是( )
①离子化合物中不一定含有金属阳离子; ②盐酸是强电解质;
③有机物中不一定都含有氢元素; ④酸酐都能直接与水反应生成相应的酸;
⑤酸性氧化物一定是非金属氧化物; ⑥有阳离子的晶体中可能没有阴离子.
①离子化合物中不一定含有金属阳离子; ②盐酸是强电解质;
③有机物中不一定都含有氢元素; ④酸酐都能直接与水反应生成相应的酸;
⑤酸性氧化物一定是非金属氧化物; ⑥有阳离子的晶体中可能没有阴离子.
| A、只有①②⑤ |
| B、只有①③⑥ |
| C、只有③⑤⑥ |
| D、只有①②④⑥ |
托盘天平左、右两盘的烧杯中各盛有100g 9.8%的稀硫酸,天平平衡,在左盘烧杯里放入5.6g Fe片,右盘里放入一定量的其他物质,充分反应后,天平仍然保持平衡,则右盘放入的物质可能是( )
| A、5.4g CuO粉末 |
| B、5.6g Cu片 |
| C、5.6g Mg条 |
| D、5.6g Zn片 |
除去下列物质中的少量杂质(括号内的物质为杂质),所选用的试剂或方法不正确的是( )
| A、Fe(OH)3胶体(FeCl3):NaOH溶液 |
| B、Cl2(HCl):饱和食盐水 |
| C、CO2(SO2):饱和NaHCO3溶液 |
| D、Na2CO3固体(NaHCO3):加热 |