题目内容
某离子反应涉及H2O、ClO—、IO3—、OH—、I2、Cl—六种微粒。其中c(ClO—)随反应进行逐渐减小。下列判断错误的是
A.该反应的还原剂是I2
B.氧化剂与还原剂的物质的量之比为5:2
C.消耗l mol氧化剂,转移2 mol电子
D.反应后溶液的碱性明显减弱
B
【解析】
试题分析:由于在反应中c(ClO—)随反应进行逐渐减小,说明ClO—是反应物,Cl—应该是生成物,由于Cl元素的化合价降低,得到电子,所以ClO—是氧化剂,还应该有还原剂失去电子,根据题中的微粒及相应元素的化合价变化可知:I2是还原剂,IO3—是氧化产物,结合电荷守恒可知,OH-是反应物,H2O是生成物,反应的方程式是:5ClO—+ I2+ 2OH—= 5Cl—+ 2IO3—+H2O。A.在该反应中I2是还原剂,所以选项A正确;B.在反应中,氧化剂ClO—与还原剂I2的物质的量之比为5:1,错误;C.根据反应前后元素的化合价的变化可知:消耗l mol氧化剂,转移2 mol电子,正确;D.由于反应不断消耗OH-,反映还产生水,所以c(OH-)增加降低,因此反应后溶液的碱性明显减弱,正确。
考点:考查微粒在氧化还原反应中的作用、性质及电子转移的知识。

下表中对应关系错误的是
A | NaCl=Na++Cl-;NH3?H2O | 均属于电离方程式 |
B | Ba2++SO42-=BaSO4↓; HCO3-+OH-=CO32-+H2O | 均可表示一类反应 |
C | SO2使酸性高锰酸钾溶液褪色; SO2使碱性酚酞溶液褪色 | 均属于SO2的同一性质 |
D | Cl2+2NaOH=NaCl+NaClO+H2O; 3S+ 6NaOH=2Na2S+Na2SO3+3H2O; | Cl2和S在反应中既作氧化剂又作还原剂 |
(16分)草酸(H2C2O4)是一种二元弱酸,部分性质如下:能溶于水,易溶于乙醇;大约在175℃升华(175℃以上分解生成H2O、CO2和CO);H2C2O4+Ca(OH)2=CaC2O4↓+2H2O。现用H2C2O4进行如下实验:
(一) 探究草酸的不稳定性
通过如图实验装置验证草酸受热分解产物中的CO2和CO,A、B、C中所加入的试剂分别是:
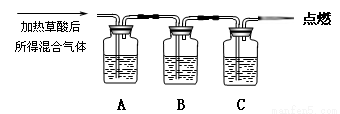
A、乙醇 B、 C、NaOH溶液。
(1)B中盛装的试剂 (填化学式)
(2)A中加入乙醇的目的是 。
(二) 探究草酸的酸性
将0.01mol草酸晶体(H2C2O4·2H2O)加入到100ml 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是 (用离子方程式表示)。
(三) 用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素
I、实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
反应原理: MnO4- + H2C2O4 + = Mn2+ + CO2↑+ H2O
(1)配平上述离子方程式。
(2)滴定时KMnO4溶液应盛装于 (填 “酸式”或“碱式”)滴定管中。
Ⅱ、探究影响化学反应速率的因素
实验组别 | c(H2C2O4) /(mol/L) | V(H2C2O4) /ml | c(KMnO4) /(mol/L) | V(KMnO4) /ml | c(H2SO4) /(mol/L) | 褪色所需时间 | 实验 目的 |
1 | 0.2 | 2 | 0.0025 | 4 | 0.12 | 6'55'' | (a) |
0.2 | 2 | 0.005 | 4 | 0.12 | 5'17'' | ||
0.2 | 2 | 0.01 | 4 | 0.12 | 3'20'' | ||
0.2 | 2 | 0.02 | 4 | 0.12 | 9'05'' | ||
0.2 | 2 | 0.03 | 4 | 0.12 | 11'33'' | ||
0.2 | 2 | 0.04 | 4 | 0.12 | 14'20'' |
下表列出了在“探究影响化学反应速率的因素”实验中得出的部分实验数据:
请回答:
(1)实验目的(a)是 ;
(2)根据表中数据在坐标中画出反应褪色所需时间随KMnO4溶液浓度的变化关系图像;
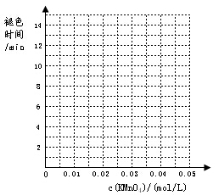
(3)若要探究催化剂对该反应速率的影响应选择MnSO4而不选MnCl2作为催化剂,其原因是 。
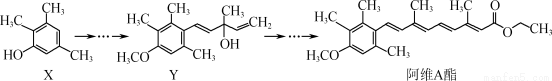


 _____(填“是”或“不是”)1—萘酚的同分异构体。
_____(填“是”或“不是”)1—萘酚的同分异构体。 NH4++OH-
NH4++OH- 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
 A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响