题目内容
12.往5000kg含KI0.3%(质量分数)的溶液中,通足量的氯气,试计算最多可得到碘单质的物质的量.分析 发生Cl2+2KI=2KCl+I2,2n(I2)=n(KI),结合n=$\frac{m}{M}$计算.
解答 解:5000kg含KI0.3%(质量分数)的溶液中,m(KI)=5000×103g×0.3%=15000g,n(KI)=$\frac{15000}{166g/mol}$=90.36mol,则由Cl2+2KI=2KCl+I2可知,n(I2)=90.36mol×$\frac{1}{2}$=45.18mol,答:最多可得到碘单质的物质的量为45.18mol.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应及物质的量计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
3.CuCl是难溶于水的白色固体,是一种重要的催化剂.工业上,由孔雀石(主要成分Cu(OH)2•CuCO3,含FeS、FeO和SiO2杂质)制备CuCl的某流程如图:
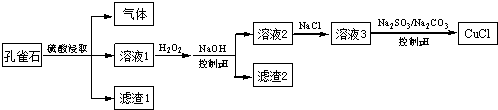
下列说法不正确的是( )

下列说法不正确的是( )
| A. | H2O2将溶液1中Fe2+氧化为Fe3+,再通过控制pH转化为Fe(OH)3除去 | |
| B. | SO32-将溶液3中的Cu2+还原,反应得到CuCl | |
| C. | CO32-作用是控制溶液pH,促使CuCl沉淀的生成 | |
| D. | 若改变试剂加入顺序,将溶液3缓慢加入到含大量SO32-/CO32-的溶液中,同样可制取CuCl |
4.将9.5g含有可溶性杂质的MgCl2全部溶于水中配制成溶液,向其中加入足量用稀硝酸酸化的AgNO3溶液,充分反应后,得到沉淀28g,则其中所含杂质不可能是( )
| A. | NaCl | B. | AlCl3 | C. | CaCl2 | D. | FeCl3 |
12.科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3.进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2、压强1.0×105 Pa、反应时间3h):
相应的热化学方程式:N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g)△H=+765.2kJ•mol-1
回答下列问题:
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注.
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议:升高温度,增大反应物N2的浓度,不断移出生成物脱离反应体系.
(3)工业合成氨的反应为N2(g)+3H2(g)高温、高压催化剂
2NH3(g).设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数为$\frac{4}{7}$.
①该条件下N2的平衡转化率为66.7%
②该条件下反应2NH3(g)高温、高压催化剂N2(g)+3H2(g)的平衡常数为0.005.
| T/℃ | 30 | 40 | 50 | 60 |
| NH3生成量/10-6 mol | 4.8 | 5.9 | 6.0 | 6.1 |

回答下列问题:
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注.
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议:升高温度,增大反应物N2的浓度,不断移出生成物脱离反应体系.
(3)工业合成氨的反应为N2(g)+3H2(g)高温、高压催化剂
2NH3(g).设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数为$\frac{4}{7}$.
①该条件下N2的平衡转化率为66.7%
②该条件下反应2NH3(g)高温、高压催化剂N2(g)+3H2(g)的平衡常数为0.005.