题目内容
4.既可以通过单质与单质化合,也可以通过溶液中的复分解反应来制得的化合物是( )| A. | FeCl3 | B. | Al2S3 | C. | CuS | D. | Fe2S3 |
分析 A、氯气是强氧化剂,将铁氧化成铁离子;
B、Al2S3只能由铝粉和硫粉化合制得,Al2S3见水就无影,易水解;
C、硫是弱氧化剂,只能将铜氧化成+1价的铜;
D、Fe和S化合生成FeS,不能生成Fe2S3,铁离子和硫离子溶液中发生氧化还原反应,不能通过盐与盐发生复分解反应得到.
解答 解:A、Fe和Cl2化合生成三氯化铁,因为氯气是强氧化剂,方程式为2Fe+3Cl2=2FeCl3,通过单质与单质化合,复分解反应也可以制备,Fe2(SO4)3+3BaCl2=2FeCl3+3BaSO4↓,故A正确;
B、Al2S3只能由铝粉和硫粉化合制得,在水溶液中不存在Al2S3,Al2S3要发生双水解,故B错误;
C、硫的氧化性弱,和铜反应只能生成硫化亚铜,故C错误;
D、Fe和S化合生成FeS,不能生成Fe2S3,铁离子和硫离子溶液中发生氧化还原反应,不能通过盐与盐发生复分解反应得到,故D错误;
故选A.
点评 本题将化学反应类型夹在元素化合物知识里考查,难度中等,对元素化合物知识有一定储备,掌握基础知识是解题关键.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
14.下列方法中不可以鉴别Fe3+和Fe2+的是( )
| A. | 通过物理方法观察他们颜色的区别 | |
| B. | 向两种溶液中加入NaOH溶液 | |
| C. | 向两种溶液中加入KSCN溶液 | |
| D. | 向两种溶液中加入氯水后再加入KSCN溶液 |
12.对可逆反应N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ.mol-1下列叙述正确的是( )
| A. | 达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大 | |
| B. | 若单位时间内消耗xmolN2,同时生成2xmolNH3,则反应达到平衡状态 | |
| C. | 若达到平衡时,共放出46.2kJ热量,则有lmo1NH3(g)生成 | |
| D. | 达到平衡后,将容器体积减小为原来的一半,重新达到平衡后,c(NH3)变为原平衡时的2倍 |
19.维生素C的结构简式如图: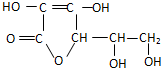 下列关于维生素C中所含官能团的说法错误的是( )
下列关于维生素C中所含官能团的说法错误的是( )
 下列关于维生素C中所含官能团的说法错误的是( )
下列关于维生素C中所含官能团的说法错误的是( )| A. | 含有羟基 | B. | 含有酯基 | C. | 含有碳碳双键 | D. | 含有醛基 |
9.已知3.01×1023个X2气体分子的质量为8g,则X2气体的摩尔质量是( )
| A. | 16 g | B. | 32 g | C. | 16g/mol | D. | 32 g/mol |
16.下列有机物或有机物组合,在现有条件下不能发生聚合反应的是( )
| A. |  和 和 | B. |  | ||
| C. |  | D. | C(CH3)4 |
14.下列表示溶液中发生反应的化学方程式错误的是( )
| A. | MnO 2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl 2+Cl 2↑+2H 2O | |
| B. | K 2Cr 2O 7+6FeSO 4+7H 2SO 4═Cr 2(SO 4) 3+3Fe 2(SO 4) 3+K 2SO 4+7H 2O | |
| C. | 2Al+2NaOH+2H 2O═2NaAlO 2+3H 2↑ | |
| D. | 2KMnO 4+HCOOK+KOH═2K 2MnO 4+CO 2↑+H 2O |
