题目内容
由CO、H2和O2组成的混和气体60mL,在一定条件下恰好完全反应,测得生成物在101kPa120℃下对氢气的相对密度为18.75,则原混和气体中H2所占的体积分数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量的相关计算
专题:计算题
分析:CO、H2和O2组成的混合气体在一定条件下恰好完全反应,生成CO2和H2O,在101kPa,120℃下对氢气的相对密度为18.75,则混合气体的平均相对分子质量为18.75×2=37.5,根据平均相对分子质量可计算CO2与H2O的物质的量的比值,根据原子守恒确定CO、H2的体积之比,根据2CO+O2=2CO2、2H2+O2=2H2O计算CO、H2的总体积,进而计算原混合气体中H2所占的体积分数.
解答:
解:CO、H2和O2组成的混合气体在一定条件下恰好完全反应,生成CO2和H2O,在101kPa,120℃下对氢气的相对密度为18.75,则混合气体的平均相对分子质量为18.75×2=37.5,
设CO2的物质的量为xmol,H2O的物质的量为ymol,
则
=37.5,
整理得x:y=3:1,
根据原子守恒n(CO):n(H2)=n(CO2):n(H2O)=3:1,
根据2CO+O2=2CO2、2H2+O2=2H2O,可知CO、H2的总体积=60mL×
=40mL,
故氢气的体积=40mL×
=10mL,
则原混合气体中H2所占的体积分数为:
=
,
故选A.
设CO2的物质的量为xmol,H2O的物质的量为ymol,
则
| 44x+18y |
| x+y |
整理得x:y=3:1,
根据原子守恒n(CO):n(H2)=n(CO2):n(H2O)=3:1,
根据2CO+O2=2CO2、2H2+O2=2H2O,可知CO、H2的总体积=60mL×
| 2 |
| 3 |
故氢气的体积=40mL×
| 1 |
| 1+3 |
则原混合气体中H2所占的体积分数为:
| 10mL |
| 60mL |
| 1 |
| 6 |
故选A.
点评:本题考查混合物的计算,难度中等,关键是根据混合气体对氢气的相对密度确定CO2与H2O的物质的量的比值,注意方程式的利用.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
NA为阿伏加德罗常数.则下列说法正确的是( )
| A、标准状况下,2.24L Cl2与热碱溶液完全反应生成Cl-和ClO3-转移了0.1NA e- |
| B、已知S-S键的键能为265kJ/mol,若使1mol某硫单质(气态)全部形成气态硫原子需要2120kJ能量,则3.2g这种硫单质中含S-S键的数目为0.1NA |
| C、0.1mol/L的FeBr3溶液中含0.3NA Br- |
| D、已知25℃,101kPa时气体摩尔体积为24.5L/mol.则此条件下0.05NA Fe与足量盐酸反应,产生H2约为1.225L |
下列方程式中,正确的是( )
| A、NaHCO3在水中电离:NaHCO3═Na++H++CO32- |
| B、CH3COOH与碳酸钙反应的离子方程式:CaCO3+2CH3COOH═H2O+Ca2++2CH3COO-+CO2↑ |
| C、乙酸乙酯在氢氧化钠作用下的化学反应方程式:CH3COOC2H5+NaOH→C2H5OH+CH3COOH |
| D、氢气燃烧的热化学方程式:2H2+O2=2H2O,△H=-571.6 kJ?mol-1 |
下列溶液中,氯离子浓度最大的是( )
| A、100mL 1mol/L的NaCl溶液 |
| B、150mL 1mol/L的MgCl2溶液 |
| C、200mL 1mol/L的HCl溶液 |
| D、10mL 1mol/L的AlCl3溶液 |
在淀粉碘化钾溶液中加入少量NaClO溶液,振荡,溶液变蓝.在上述溶液中加入足量的Na2SO3溶液,蓝色逐渐消失.下列判断错误的是( )
| A、氧化性:ClO->I2 |
| B、蓝色逐渐消失说明Na2SO3具有漂白性 |
| C、漂白粉溶液可使淀粉碘化钾试纸变蓝 |
| D、向新制氯水中加入足量亚硫酸钠溶液,氯水褪色 |
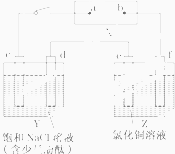 如图X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.
如图X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.