题目内容
计算下列物质的摩尔质量
NaCl KNO3 CuSO4?5H2O 氢氧化钠 硫酸 氯化镁 .
NaCl
考点:摩尔质量
专题:化学用语专题
分析:摩尔质量以g/mol作单位数值上等于其相对分子质量,相对分子质量为构成分子的各原子的相对原子质量之和,据此解答.
解答:
解:NaCl的化学式可知相对分子质量=23+35.5=58.5,摩尔质量=58.5g/mol;
KNO3 化学式可知相对分子质量=39+14+3×16=101,摩尔质量为101g/mol;
由晶体的化学式CuSO4?5H2O知,该晶体的相对分子质量为:64+32+16×4+5×(1×2+16)=250,其摩尔质量为250g/mol;
氢氧化钠化学式为NaOH,相对分子质量=23+16+1=40,摩尔质量为40g/mol;
由硫酸的化学式H2SO4知,硫酸的相对分子质量=1×2+32+16×4=98,其摩尔质量为98g/mol;
氯化镁化学式为MgCl2,相对分子质量=24+35.5×2=95g/mol;
故答案为:58.5g/mol,101g/mol,250g/mol,40g/mol,98g/mol,95g/mol.
KNO3 化学式可知相对分子质量=39+14+3×16=101,摩尔质量为101g/mol;
由晶体的化学式CuSO4?5H2O知,该晶体的相对分子质量为:64+32+16×4+5×(1×2+16)=250,其摩尔质量为250g/mol;
氢氧化钠化学式为NaOH,相对分子质量=23+16+1=40,摩尔质量为40g/mol;
由硫酸的化学式H2SO4知,硫酸的相对分子质量=1×2+32+16×4=98,其摩尔质量为98g/mol;
氯化镁化学式为MgCl2,相对分子质量=24+35.5×2=95g/mol;
故答案为:58.5g/mol,101g/mol,250g/mol,40g/mol,98g/mol,95g/mol.
点评:本题考查了摩尔质量的计算,明确摩尔质量与相对分子质量的关系是解本题关键,题目难度不大.

练习册系列答案
相关题目
将2mol/l SO2和1mol/l的O2在在密闭容器中混合并在一定条件下反应2SO2+O2?2SO3若2s后测得SO3的浓度为0.6mol/l,则SO2平均化学反应速率为是( )
| A、v(SO2)=0.3 mol/(L?s) |
| B、v(SO2)=0.15 mol/(L?s) |
| C、v(SO2)=0.6 mol/(L?s) |
| D、v(SO2)=0.5 mol/(L?s) |
下列关于药物的使用说法正确的是( )
| A、虽然药物能治病,但大部分药物有毒副作用 |
| B、毒品就是有毒的药品 |
| C、长期大量使用阿司匹林可预防疾病,没有副作用 |
| D、OTC表示处方药,R表示非处方药 |
1克N2含有N个分子,则阿伏加德罗常数是( )
| A、14N | ||
B、
| ||
| C、28N | ||
D、
|
由CO、H2和O2组成的混和气体60mL,在一定条件下恰好完全反应,测得生成物在101kPa120℃下对氢气的相对密度为18.75,则原混和气体中H2所占的体积分数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、1.2 g镁在足量的氮气中燃烧,镁失去的电子数为0.2NA |
| B、0.1 mol/L氢氧化钠溶液中所含Na+数为0.1NA |
| C、11.2 L二氧化碳中所含有的氧原子数为NA |
| D、46g NO2和N2O4的混合气体中含有的原子个数为3NA |
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是有机物.
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是有机物.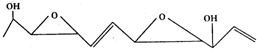 已知:
已知: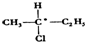 就有光学活性.标有“*”号的碳原子叫手性碳原子.
就有光学活性.标有“*”号的碳原子叫手性碳原子.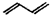 .
.