题目内容
(1)常温下将0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+) 0.2mol/LHCl溶液中由水电离出的c(H+); (填“>”、“<”、或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)= mol/L;
c(H+)-c(MOH)= mol/L.
(2)常温下若将0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度 MCl的水解程度.(填“>”、“<”、或“=”)
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH .(填“>7”、“<7”、或“无法确定”)
①混合溶液中由水电离出的c(H+)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)=
c(H+)-c(MOH)=
(2)常温下若将0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:(1)①酸或碱能抑制水电离,含有弱根离子的盐促进水电离;
②根据物料守恒和电荷守恒分析;
(2)二者混合得到等物质的量浓度的MCl和MOH,混合溶液呈酸性,说明碱的电离程度小于盐的水解程度;
(3)pH=3的HR溶液与pH=11的NaOH溶液,两种溶液中c(H+)=c(OH-),如HR为强酸,则反应后呈中性,如为弱酸,则反应后呈酸性.
②根据物料守恒和电荷守恒分析;
(2)二者混合得到等物质的量浓度的MCl和MOH,混合溶液呈酸性,说明碱的电离程度小于盐的水解程度;
(3)pH=3的HR溶液与pH=11的NaOH溶液,两种溶液中c(H+)=c(OH-),如HR为强酸,则反应后呈中性,如为弱酸,则反应后呈酸性.
解答:
解:(1)①酸或碱能抑制水电离,含有弱根离子的盐促进水电离,所以混合溶液中由水电离出的c(H+)>0.2mol/LHCl溶液中由水电离出的c(H+),
故答案为:>;
②根据电荷守恒得c(Cl-)+c(OH-)=c(M+)+c(H+),所以:c(Cl-)-c(M+)=c(H+)-c(OH-)=10-6 mol/L-10-8mol/L=9.9×10-7mol/L;
c(M+)+c(MOH)=0.1mol/L=c(Cl-),c(H+)-c(MOH)=c(OH-)=10-8mol/L,
故答案为:9.9×10-7;10-8;
(2)二者混合得到等物质的量浓度的MCl和MOH,混合溶液呈酸性,说明碱的电离程度小于盐的水解程度,
故答案为:<;
(3)HR若为强电解质,二者都是一元酸或碱,等体积混合后溶液的pH=7,而混合溶液的pH≠7,说明HR为弱电解质,二者混合后溶液中酸过量,反应后溶液显示酸性,溶液pH<7,
故答案为:<7.
故答案为:>;
②根据电荷守恒得c(Cl-)+c(OH-)=c(M+)+c(H+),所以:c(Cl-)-c(M+)=c(H+)-c(OH-)=10-6 mol/L-10-8mol/L=9.9×10-7mol/L;
c(M+)+c(MOH)=0.1mol/L=c(Cl-),c(H+)-c(MOH)=c(OH-)=10-8mol/L,
故答案为:9.9×10-7;10-8;
(2)二者混合得到等物质的量浓度的MCl和MOH,混合溶液呈酸性,说明碱的电离程度小于盐的水解程度,
故答案为:<;
(3)HR若为强电解质,二者都是一元酸或碱,等体积混合后溶液的pH=7,而混合溶液的pH≠7,说明HR为弱电解质,二者混合后溶液中酸过量,反应后溶液显示酸性,溶液pH<7,
故答案为:<7.
点评:本题考查了酸碱混合的定性判断及有关pH的计算,题目难度中等,注意掌握电荷守恒、物料守恒、质子守恒的含义及应用方法,明确酸碱混合的定性判断方法及溶液pH的计算方法.

练习册系列答案
相关题目
在298K时,NaCl在水中的溶解度为36g.若将1mol NaCl溶解在1L水中,此溶解过程中体系的△H-T△S和△S如何变化( )
| A、△H-T△S>0,△S<0 |
| B、△H-T△S<0,△S>0 |
| C、△H-T△S>0,△S>0 |
| D、△H-T△S<0,△S<0 |
A、B分别是M元素的碳酸盐和碳酸氢盐,将一定量A、B的混合物与足量盐酸反应,消耗HCl与CO2的物质的量之比为3:2.已知M可能是ⅠA族或ⅡA族元素,则混合物中A、B的物质的量之比可能是( )
| A、3:1 | B、2:1 |
| C、1:2 | D、1:4 |
下列操作中正确的是( )
A、 |
B、 |
C、 |
D、 |
短周期元素X、Y、Z在周期表中的位置关系如图,则三种元素可能是( )
| X | ||
| Y | ||
| Z |
| A、C Al Ca |
| B、He F S |
| C、Al Ca Rb |
| D、O P Ge |

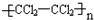 B.
B.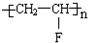 C.
C.