题目内容
7.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )| A. | 1 molN2与4 mol H2反应生成的NH3分子数为2NA | |
| B. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| C. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA | |
| D. | 11.2 L标况下的SO3所含分子数为0.5NA |
分析 A、合成氨的反应为可逆反应;
B、铁溶于过量的硝酸后变为+3价;
C、乙烯、丙烯和丁烯的最简式均为CH2;
D、标况下三氧化硫为固体.
解答 解:A、合成氨的反应为可逆反应,不能进行彻底,故生成的氨气分子小于2NA个,故A错误;
B、铁溶于过量的硝酸后变为+3价,1mol铁转移3NA个电子,故B错误;
C、乙烯、丙烯和丁烯的最简式均为CH2,故14g混合物中含1molCH2,故含3NA个原子,故C正确;
D、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量和含有的分子个数,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
17.一定温度下在一容积恒定的密闭容器中,进行如下可逆反应:A(s)+4B(g)?3C(g)+D (g).能表明该反应已达到平衡状态的是( )
| A. | 4V正(B)=3V逆(C) | |
| B. | 单位时间消耗n mol A,同时生成3n mol C | |
| C. | 容器内气体的分子数目不变 | |
| D. | A的转化率达到最大值 |
18.下列元素肯定属于主族元素的是( )
| A. | 最高正价为+7价的一种元素 | |
| B. | 最外电子数为2的元素 | |
| C. | 原子L层比M层多6个电子的一种元素 | |
| D. | 最外层电子数为8的一种元素 |
2.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红的溶液中:Na+、Cl-、CH3COO-、Fe2+ | |
| B. | 水电离的OH-浓度为10-12mol/L的溶液中:Mg2+、NH4+、AlO2-、SO32- | |
| C. | 无色溶液中:Al3+、NO3-、Cl-、SO42- | |
| D. | c(K2C2O4)=0.5mol/L溶液中:Na+、K+、MnO4-、Cl- |
12.下列各组中的离子,能在溶液中大量共存的是( )
| A. | K+、Cu2+、Cl-、OH- | B. | Mg2+、SO42-、K+、Cl- | ||
| C. | Na+、H+、NO3-、CO32- | D. | Ba2+、Na+、OH-、SO42- |
19.在K2SO4、KCl、KNO3的混合溶液中,含有K+、SO42-、Cl-、NO3-,已知其中K+、SO42-、NO3-的个数比为8:1:2,则溶液中K2SO4、KCl、KNO3的“分子”个数比为( )
| A. | 1:1:1 | B. | 1:4:2 | C. | 1:2:4 | D. | 1:3:2 |
17.下列反应的离子方程式正确的是( )
| A. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 碳酸钙溶于稀盐酸中 CO32─+2H+═CO2↑+H2O | |
| C. | 碳酸氢钠溶液与盐酸反应 HCO3─+H+═CO2↑+H2O | |
| D. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag |
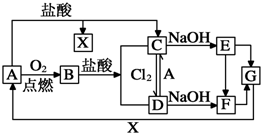 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题. .
.