题目内容
20.下列说法中错误的是( )| A. | CS2、SO3、P4和C6H6都是非极性分子 | |
| B. | 在H3O+和[Cu(H2O)4]2+中都存在配位键 | |
| C. | 元素电负性越大的原子,该元素的原子吸引键合电子的能力越强 | |
| D. | 在电中性晶体中只要含有阳离子,则一定含有阴离子 |
分析 A、对于ABn型共价分子,若中心原子A达到了最高正价,没有孤对电子时,为非极性分子,若中心原子未达到最高正价,有孤对电子对,为极性分子;
B、配位键形成条件:一是中心原子或离子,它必须有能接受电子对的空轨道;二是配位体,组成配位体的原子必须能提供配对的孤对电子;
C、电负性是元素的原子在化合物中吸引电子能力的标度,电负性越大,表示该元素的非金属性越强;
D、在电中性晶体中只要含有阳离子,不一定含有阴离子,例如金属晶体只有阳离子和自由电子.
解答 解:A、CS2中心原子C的化合价为+4价,最外层电子全部参与成键,不含有孤对电子对,为非极性分子;SO3中心原子S的化合价为+6价,最外层电子全部参与成键,没有孤对电子对,SO3是平面三角形的分子,是非极性分子,P4中都是非极性键,所以是非极性分子,C6H6分子是中心对称结构,是非极性分子,故A正确;
B、水分子与氢离子通过配位键形成H3O+,铜离子提供空轨道,氨气分子提供孤对电子对,Cu2+与NH3通过配位键形成[Cu(NH3)4]2+,故B正确;
C、电负性是元素的原子在化合物中吸引电子能力的标度,元素电负性数值越大,表示其原子在化合物中吸引电子的能力越强;反之,电负性数值越小,相应原子在化合物中吸引电子的能力越弱,故C正确;
D、在电中性晶体中只要含有阳离子,不一定含有阴离子,例如金属晶体只有阳离子和自由电子,故D错误;
故选:D.
点评 综合性较大,涉及分子极性、配位键、电负性、晶体结构与性质,难度不大,注意基础知识的掌握.

练习册系列答案
相关题目
8.电解水﹙H2O﹚和重水﹙D2O﹚的混合物,通电一定时间后,两极共生成气体18.5克,体积为33,6L﹙标况﹚,所生成的气体中重氢﹙D﹚和普氢﹙H﹚的原子个数比是( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
15.通常人们把拆开1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看成该化学键的键能.已知热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol请根据热化学方程式和表中数据计算N≡N键的键能x约为( )
| 化学键 | H-H | N≡N | H-N |
| 键能 | 436 kJ/mol | x | 391kJ/mol |
| A. | 431kJ/mol | B. | 946kJ/mol | C. | 649kJ/mol | D. | 869kJ/mol |
5.中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是( )
| A. | 根据氧化还原反应的规律,推出强氧化剂遇到强还原剂一定会发生氧化还原反应 | |
| B. | 根据化学反应的规律,推出氢氧化铁可通过化合反应得到 | |
| C. | 根据元素的非金属性较强,其单质也越活泼规律,推出磷单质比N2稳定得多 | |
| D. | 根据CO2通入Ba(NO3)2溶液中无沉淀的规律推测,SO2入Ba(NO3)2溶液中也无沉淀产生 |
9.下列标明电子转移的方向和数目的化学方程式中正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  第II卷(非选择题,共50分) |
10.已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H=+489.0kJ•mol-1①
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1②
C(石墨)+O2(g)═CO2(g)△H=-393.5kJ•mol-1③
则4Fe(s)+3O2(g)═2Fe2O3(s)的△H为( )
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1②
C(石墨)+O2(g)═CO2(g)△H=-393.5kJ•mol-1③
则4Fe(s)+3O2(g)═2Fe2O3(s)的△H为( )
| A. | +1 164.1 kJ•mol-1 | B. | -1 641.0 kJ•mol-1 | ||
| C. | -259.7 kJ•mol-1 | D. | -519.4 kJ•mol-1 |
 过氧化氢的电子式
过氧化氢的电子式
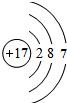 ,其最高价氧化物对应的水化物的化学式为HClO4.
,其最高价氧化物对应的水化物的化学式为HClO4.