��Ŀ����
9����ҩ�Ŀ�����ҩ��ϳ����л���ѧ�о���Ҫ��չ����ijҩ��V�ĺϳ�·����ͼ��
��1��II�к��������ŵ�����ȩ����
��2����Ӧ�ڵĻ�ѧ����ʽ2
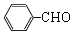 +O2$��_{��}^{����}$2
+O2$��_{��}^{����}$2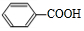 ��
����3��I��III��Ũ���������ʱ��Ӧ�Ļ�ѧ����ʽ
 +
+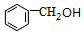 $?_{��}^{Ũ����}$
$?_{��}^{Ũ����}$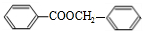 +H2O��
+H2O����4������˵����ȷ����BC��
A��I��V�����ڷ����� B��II�ܷ���������Ӧ
C��lmolII��4molH2�����ӳɷ�Ӧ D����Ӧ������������Ӧ
��5����Ӧ�۵ķ�Ӧ����ȡ����Ӧ��A�ķ���ʽC9H13ON
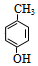
��6����I��Ϊͬ���칹��ķ����廯���ﹲ��4�֣�����VI��FeCl3������ɫ��Ӧ���䱽���ϵ�һ�ȴ���ֻ��2�֣�д����������������VI�Ľṹ��ʽ
 ��
����7��һ�������£�������VII
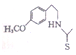 Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ��VII�Ļ�������Ľṹ��ʽ
Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ��VII�Ļ�������Ľṹ��ʽ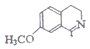 ��
��
���� ����I��II�ṹ��ʽ֪��I������������Ӧ����II��II����������Ӧ����III��III��A��Ӧ����IV����IV�ṹ��ʽ֪���÷�Ӧ��ȡ����Ӧ��A�ṹ��ʽΪ ��IV������ȥ��Ӧ����V�������Ŀ�������
��IV������ȥ��Ӧ����V�������Ŀ�������
��� �⣺����I��II�ṹ��ʽ֪��I������������Ӧ����II��II����������Ӧ����III��III��A��Ӧ����IV����IV�ṹ��ʽ֪���÷�Ӧ��ȡ����Ӧ��A�ṹ��ʽΪ ��IV������ȥ��Ӧ����V��
��IV������ȥ��Ӧ����V��
��1�����ݽṹ��ʽ֪��II�к��������ŵ�����ȩ�����ʴ�Ϊ��ȩ����
��2����Ӧ�ڵķ�Ӧ���DZ���ȩ����������Ӧ�����Ǵ��������ȣ���÷�Ӧ�Ļ�ѧ����ʽ2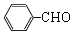 +O2$��_{��}^{����}$2
+O2$��_{��}^{����}$2 ��
��
�ʴ�Ϊ��2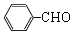 +O2$��_{��}^{����}$2
+O2$��_{��}^{����}$2 ��
��
��3��I�DZ��״���III�DZ����ᣬI��III��Ũ���������ʱ����������Ӧ���ɱ����ᱽ��������÷�Ӧ�Ļ�ѧ����ʽ +
+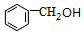 $?_{��}^{Ũ����}$
$?_{��}^{Ũ����}$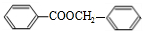 +H2O��
+H2O��
�ʴ�Ϊ�� +
+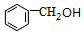 $?_{��}^{Ũ����}$
$?_{��}^{Ũ����}$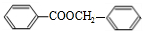 +H2O��
+H2O��
��4��A��I��V�ж�����C��H��OԪ����V������NԪ�أ����Զ��߶������ڷ���������A����
B��II�к���ȩ������II�ܷ���������Ӧ����B��ȷ��
C��������ȩ�����ܺ����������ӳɷ�Ӧ������lmolII��4molH2�����ӳɷ�Ӧ����C��ȷ��
D����Ӧ������ȡ����Ӧ����D����
��ѡBC��
��5����Ӧ�۵ķ�Ӧ������ȡ����Ӧ��A�ṹ��ʽΪ ����A�ķ���ʽΪC9H13ON��
����A�ķ���ʽΪC9H13ON��
�ʴ�Ϊ��ȡ����C9H13ON��
��6����I��Ϊͬ���칹��ķ����廯���˵��I��ͬ���칹���к��б�����������з��ǻ��ͼ�������3�ֽṹ����������Ѽ�������һ�ֽṹ�����Է��������Ĺ���4�֣�����VI��FeCl3������ɫ��Ӧ��˵�����з��ǻ����䱽���ϵ�һ�ȴ���ֻ��2�֣�˵�����ǻ��ͼ����ڶ�λ����������������VI�Ľṹ��ʽΪ ��
��
�ʴ�Ϊ��4�� ��
��
��7��һ�������£�������VII  Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ��VII�Ļ�������Ľṹ��ʽΪ
Ҳ�ܷ������Ʒ�Ӧ�ܵĻ�����Ӧ��VII�Ļ�������Ľṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л��ϳɺ��л��ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ���������жϼ�֪ʶǨ����������ȷ�жϷ�Ӧ�жϼ��ͳɼ�λ�ü��ص��ǽⱾ��ؼ���ע�ⷴӦ���л�ѧ���仯����Ŀ�Ѷ��еȣ�

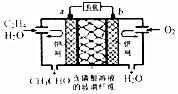 ��ʯ����2012�꽫���120��ֵ���ϩ�����仧���죬��ϩ���л�������ҵ����Ҫԭ�ϣ��кܶ���Ҫ��;���磺��ϩ����������ȩ����Ƴ�����ͼ��ʾ��ȼ�ϵ�أ����Ʊ���ȩ��ͬʱ���ɻ�õ��ܣ����ܷ�Ӧ��ѧ����ʽΪ��2CH2�TCH2+O2��2CH3CHO�������й�˵����ȷ���ǣ�������
��ʯ����2012�꽫���120��ֵ���ϩ�����仧���죬��ϩ���л�������ҵ����Ҫԭ�ϣ��кܶ���Ҫ��;���磺��ϩ����������ȩ����Ƴ�����ͼ��ʾ��ȼ�ϵ�أ����Ʊ���ȩ��ͬʱ���ɻ�õ��ܣ����ܷ�Ӧ��ѧ����ʽΪ��2CH2�TCH2+O2��2CH3CHO�������й�˵����ȷ���ǣ�������| A�� | �õ�ص缫aΪ������bΪ���� | |
| B�� | �����ƶ����缫a��������Һ���缫b | |
| C�� | ������ӦʽΪ��CH2�TCH2-2e-+H2O�TCH3CHO+2H+ | |
| D�� | b�缫��2.24LO2��Ӧ����Һ����0.4molH+Ǩ�Ƶ�b�缫�Ϸ�Ӧ |
| A�� | NaHSO3����ˮ�����ԣ�NaHSO3�TNa++H++SO32- | |
| B�� | ��Na2S2O3��Һ�еμ�ϡ���2H++S2O32-�TSO2��+S��+H2O | |
| C�� | Ũ������MnO2��Ӧ��������MnO2+4HCl�TMn2++2Cl2+2H2O | |
| D�� | ��ҵұ��Mg��2Mg2++2O2-$\frac{\underline{\;���\;}}{\;}$2Mg+O2�� |
| A�� | �ռ��������ű���ʳ��ˮ�ķ��� | |
| B�� | ��ѹ������������SO2��O2��Ӧ����SO3 | |
| C�� | ��NO2���������ˮ����ɫ���� | |
| D�� | �Ӵ�����ʹN2��H2��һ����������ת��ΪNH3 |
| A�� | ͬ����������A������B������������Ŀ֮��Ϊa��b | |
| B�� | ����A������B��Ħ������֮��Ϊa��b | |
| C�� | ��ͬ�����£�a g����A��b g����B���֮��Ϊb��a | |
| D�� | ��ͬ�����£�����A������B���ܶ�֮��Ϊb��a |
| A�� | ���ǡ����ᱵ��ˮ�ֱ����ڷǵ���ʡ�ǿ����ʺ�������� | |
| B�� | �����г�������þ����������ͭ�Ⱦ���ͨ���Ȼ�ԭ��ұ�� | |
| C�� | ������н����ԣ�����Ϊͬ�ֽ������ӵ��˶��й��ɣ��������˶� | |
| D�� | ����2NO+2CO?2CO2+N2�ġ�H��0����÷�Ӧһ�����Է����� |
 �£�N2H4���Ͱ��ǵ������ֳ���������ڿ�ѧ�������������й㷺Ӧ�ã��ش��������⣺
�£�N2H4���Ͱ��ǵ������ֳ���������ڿ�ѧ�������������й㷺Ӧ�ã��ش��������⣺��1��N2H4��Nԭ�Ӻ��������ﵽ8�����ȶ��ṹ��д��N2H4�Ľṹʽ��
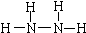 ��
����2��ʵ���������ֹ�����ȡNH3�ķ�Ӧ��ѧ����ʽΪ2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2H2O+2NH3����
��3��NH3��NaClO��Ӧ�ɵõ��£�N2H4�����÷�Ӧ�Ļ�ѧ����ʽΪ2NH3+NaClO=N2H4+NaCl+H2O��
��4����һ����ȼ�ϵ����һ�ּ��Ի�����أ��õ�طŵ�ʱ�������ķ�ӦʽΪN2H4+4OH--4e-=N2+4H2O��
��5����ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO��NH2��2]��Ӧ�Ļ�ѧ����ʽΪ2NH3��g��+CO2��g��?CO��NH2��2��l��+H2O��l�����÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ�����
| T/�� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
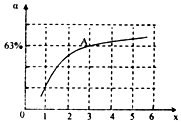
����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2�����ʵ���֮�ȣ���̼�ȣ�[n��NH3����n��CO2]=x����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ����c��NH3������ƽ�������ƶ���ͼ��A�㴦��NH3��ƽ��ת����Ϊ42%��
| n��N2�� | n��H2�� | n��NH3�� | |
| �� | 1mol | 3mol | 0mol |
| �� | 0.5mol | 1.5mol | 1mol |
| �� | 0mol | 0mol | 4mol |
���ж��������з�Ӧ���еķ��������������������ƶ���
�ڴ�ƽ��ʱ���ס��ҡ�����������NH3�����������С˳��Ϊ������=�ң�
��7�������ڴ�����ȼ�գ�����һ�ֵ��ʺ�ˮ����д���÷�Ӧ�Ļ�ѧ����ʽ��4NH3+5O2$\frac{\underline{\;��ȼ\;}}{\;}$2N2+6H2O����ѧ�����ô�ԭ������Ƴɰ���һ����ȼ�ϵ�أ���ͨ�백���ĵ缫�Ǹ��� ����������������������������£��õ缫������Ӧ�ĵ缫��ӦʽΪ2NH3-6e-+6OH-=N2+6H2O��
��8��һ�������£�ij�ܱ������з�����Ӧ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g������һ��������ܱ������У�Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ������д�ʩ�пɲ��õ���c������ĸ���ţ���
a������ѹǿ b���ʵ������¶� c������O2��Ũ�� d��ѡ���Ч����
��9�����ij��ˮ�ĵ���̶�Ϊ1%��Ũ��Ϊ0.01mol/LMgCl2��Һ�μӰ�ˮ����ʼ��������ʱ����������Һ����仯������Һ�е�NH3•H2O��Ũ��Ϊ0.002mol/L[��֪Ksp[Mg��OH��2]=4.0��10-12]��
| A�� | CH3CH2CH3 | B�� | CH3CH2CH2CH3 | C�� | CH3COCH2CH3 | D�� |  |
 �����Dz�ͬ�¶���ˮ�����ӻ������ݣ�
�����Dz�ͬ�¶���ˮ�����ӻ������ݣ�| �¶�/�� | 25 | t1 | t2 |
| ˮ�����ӻ� | 1��10-14 | a | 1��10-12 |
��1����25��t1��t2����a�������������������=����1��10-14
��2����t2�¶��²��ij��ҺpH=7������Һ�Լ��ᡱ��������С����ԣ�
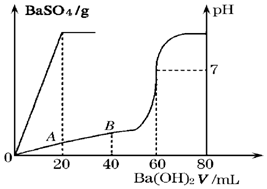
��3��25��ʱ�������������Ļ��Һ20mL������0.05mol•L-1��Ba��OH��2��Һʱ������BaSO4����������Һ��pH������ͼ��ʾ�ı仯��
���ԭ���Һ���������������ʵ���Ũ�ȷֱ��ǣ�c��H2SO4��=0.05 mol•L-1��c��HCl��=0.2 mol•L-1
����A��ʱ��pH=1 ������Һ��Ϻ�������䣩