题目内容
10.用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),从而可知M的相对原子质量为( )| A. | 2.5 ax/b | B. | 5.6 ax/b | C. | 11.2 ax/b | D. | 22.4 ax/b |
分析 根据电解时,得失电子数相等推断金属与氧气的关系,从而确定金属的原子量.
解答 解:设M的原子量为R,
电解时,电池反应方程式为:4M(NO3)x+2xH2O$\frac{\underline{\;通电\;}}{\;}$4M+xO2↑+4xHNO3
4Rg 22.4xL
ag bL
所以R=$\frac{5.6ax}{b}$,
故选B.
点评 本题以电解原理为载体考查了氧化还原反应的有关计算,能正确写出该电池的电池反应式并找出金属与氧气的关系式是解本题的关键,要注意根据得失电子相等配平方程式,才能正确解答问题.

练习册系列答案
相关题目
20.下列说法中正确的是( )
| A. | 在相同条件下,燃烧等物质的量的C2H4和乙醇,消耗O2体积不相同 | |
| B. | 分子式为C7H8O且属于酚类物质的同分异构体有4种 | |
| C. | 室温下,在水中的溶解度:乙醇>苯酚>乙酸乙酯 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼 |
1.下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A. | 酸性氧化物 干冰 SO2 | B. | 碱 苛性钠 NaOH | ||
| C. | 盐 钡餐 BaCO3 | D. | 单质 氯水 Cl2 |
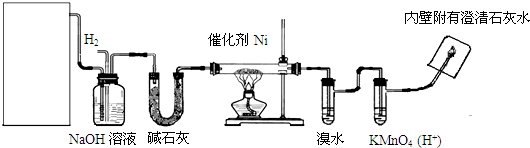
5.下列叙述正确的是( )
| A. | 装置Ⅰ在反应过程中自始至终只生成红棕色气体 | |
| B. | 装置Ⅱ开始阶段铁丝只发生析氢腐蚀 | |
| C. | 装置Ⅱ在反应过程中能产生氢气 | |
| D. | 装置Ⅰ在反应结束时溶液中的金属阳离子只有Cu2+ |
15.含苯酚的工业废水处理的流程图细下图所示,下列说法不确的是( )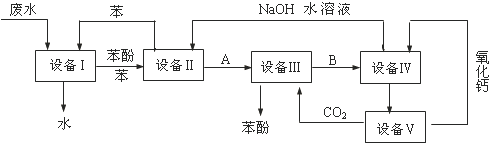

| A. | 上述流程里,设备Ⅰ、Ⅱ中进行的是分液操作;实验室里该操作可以用分液漏斗进行 | |
| B. | 上述流程里,设备Ⅲ、Ⅳ中进行的是过滤操作;实验室里该操作用到的玻璃仪器有:漏斗、烧杯、玻璃棒 | |
| C. | 在设备Ⅲ中发生反应的化学方程式为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 | |
| D. | 图中循环使用的物质是C6H6、CaO、CO2和NaOH |
2.烯烃、炔烃、芳香烃和乙醛都能发生加成反应.这是因为它们都含有( )
| A. | 单键 | B. | 不饱和碳原子 | C. | 非极性键 | D. | 碳原子 |
19.《后汉书•郡国志》中记载:“石出泉水…其水有肥,燃之极明,不可食,县人谓之石漆.”《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明.”这里的“石漆”“石脂水”是指( )
| A. | 油脂 | B. | 油漆 | C. | 石油 | D. | 煤焦油 |
9.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑩九种元素在周期表中的位置.
请回答:(以下用相应的元素符号回答问题)
(1)在表里填写①~⑩元素符号,写出元素符号①H、③Mg、⑧Cl.
(2)其中化学性质最不活泼的是He(填元素符号).
(3)在②、③、④三种元素的氧化物对应的水化物中,碱性最强的是NaOH(填化学式).
(4)元素①、②、⑤按原子半径由大到小的顺序依次为K>Na>H(填元素符号)
(5)元素⑥的氢化物的化学式是NH3,该氢化物溶于水,所得溶液的pH>(填“<”、“>”或“=”)7.
(6)元素②与元素⑧形成的化合物的电子式是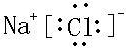 ,高温下灼烧该化合物火焰呈黄色.
,高温下灼烧该化合物火焰呈黄色.
(7)Al(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | O |
| 1 | ① | ⑩ | ||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑤ | ⑨ |
(1)在表里填写①~⑩元素符号,写出元素符号①H、③Mg、⑧Cl.
(2)其中化学性质最不活泼的是He(填元素符号).
(3)在②、③、④三种元素的氧化物对应的水化物中,碱性最强的是NaOH(填化学式).
(4)元素①、②、⑤按原子半径由大到小的顺序依次为K>Na>H(填元素符号)
(5)元素⑥的氢化物的化学式是NH3,该氢化物溶于水,所得溶液的pH>(填“<”、“>”或“=”)7.
(6)元素②与元素⑧形成的化合物的电子式是
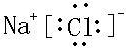 ,高温下灼烧该化合物火焰呈黄色.
,高温下灼烧该化合物火焰呈黄色.(7)Al(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应.