题目内容
16.下列各分子中所有原子都满足最外层为8电子结构的是( )| A. | N2 | B. | BF3 | C. | PCl5 | D. | HCl |
分析 对ABn型分子,最外层电子数+|化合价|=8,则满足所有原子都满足最外层8电子结构,含有H元素的化合物中H元素一定不满足8电子结构以此进行分析.
解答 解:A.N2中,N与N原子之间有3个共用电子对,则N原子的最外层电子为5+3=8,满足8电子稳定结构,故A正确;
B.BF3中,B原子的最外层电子为3个,化合价为+3价,3+3=6,所以不满足所有原子最外层为8电子结构,故B错误;
C.PCl5中,P原子的最外层电子为5个,化合价为+5,5+5=10,Cl原子的最外层电子为7个,化合价为-1价,7+|-1|=8,不都满足8电子稳定结构,故C错误;
D.HCl中H元素化合价为+1,H原子最外层电子数为1,所以1+1=2,H原子不满足8电子结构,故D错误;
故选A.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列化学反应的离子方程式正确的是( )
| A. | 用醋酸除去水垢:2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑ | |
| B. | 硫酸铁溶液中通入硫化氢气体:2Fe3++3H2S→2FeS↓+S↓+6H+ | |
| C. | 铝与氢氧化钠溶液反应:Al+2OH-→AlO2-+H2↑ | |
| D. | 已知25℃时,电离常数Ki (苯甲酸)>Ki1(H2CO3)>Ki (苯酚)>Ki2(H2CO3).常温下将水杨酸(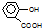 )与过量的Na2CO3溶液混合: )与过量的Na2CO3溶液混合: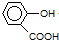 +2CO32-→ +2CO32-→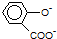 +2HCO3- +2HCO3- |
11.下列有关硅的叙述中,不正确的是( )
| A. | 硅胶可用作袋装食品干燥剂 | |
| B. | 纯净的SiO2可以制备光导纤维 | |
| C. | 硅酸盐一般易溶于水,化学性质很稳定 | |
| D. | 晶体硅是良好的半导体材料,可用于制造计算机芯片 |
1.下列各组物质在溶液中的反应,无论反应物的量多少,都能用同一离子方程式表示的是( )
| A. | Ba(OH)2与H2S04 | B. | FeBr2与Cl2 | C. | HCI与Na2CO3 | D. | NaHC03与Ca(OH)2 |
5.设NA代表阿加德罗常数,下列说法正确的是( )
| A. | 1L 1mol/L醋酸溶液中离子总数为2NA | |
| B. | 常温常压下,4.6 g NO2气体含有0.1NA个分子 | |
| C. | 常温下,1L0.50mol•L-1NH4Cl溶液与2L0.25 mol•L-1NH4Cl溶液含NH4+物质的量不同 | |
| D. | l mol•L-1的NaClO溶液中ClO-和HClO共NA个 |
6.下列能源属于二次能源的是( )
| A. | 煤 | B. | 风力 | C. | 电力 | D. | 石油 |
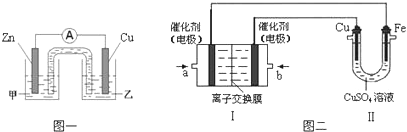

 .
. ,F1的结构简式是
,F1的结构简式是 .
.