题目内容
4.原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等:X能分别与Y、Z能形成10电子的化合物,常温下Y与X形成的是一种刺激性气味的气体,X与Z形成化合物是一种液体.下列说法正确的是( )| A. | Y、Z分别与X形成的氢化物含有一种特殊的化学键即氢键 | |
| B. | W的氯化物水溶液中通入过量YX3气体会出现先沉淀后沉淀溶解的现象 | |
| C. | 由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度 | |
| D. | 已知YX3形成的水溶液能导电,说明YX3是一种电解质 |
分析 原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,则可能为H、Be、Al;X能分别与Y、Z能形成10电子的化合物,常温下Y与X形成的是一种刺激性气味的气体,该气体为氨气,则X为H、Y为N元素;X与Z形成化合物是一种液体,该化合物为水,则Z为O元素;结合原子序数W大于O可知,W为Al元素,据此结合元素周期律知识解答.
解答 解:原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,则可能为H、Be、Al;X能分别与Y、Z能形成10电子的化合物,常温下Y与X形成的是一种刺激性气味的气体,该气体为氨气,则X为H、Y为N元素;X与Z形成化合物是一种液体,该化合物为水,则Z为O元素;结合原子序数W大于O可知,W为Al元素,
A.Y、Z分别为N、O元素,二者的氢化物氨气、水分子中都含有氢键,但是氢键属于分子间作用力,不属于化学键,故A错误;
B.氨水为弱碱,氯化铝与氨水反应生成氢氧化铝沉淀,氨水过量时氢氧化铝不溶解,故B错误;
C.X、Y、Z分别为H、N、O,三种元素组成盐为硝酸铵,硝酸铵水溶液中铵根离子部分水解,溶液呈酸性,导致铵根离子浓度小于酸根离子,故C正确;
D.YX3为NH3,氨气溶于水形成氨水,氨水能够导电,但导电离子不是氨气电离的,氨气为非电解质,故D错误;
故选C.
点评 本题考查了原子结构与元素周期律的关系,题目难度不大,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题有利于提高学生的分析能力及逻辑推理能力.

练习册系列答案
相关题目
14.下列离子方程式中书写不正确的是( )
| A. | 大理石与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 水玻璃中加入稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ | |
| C. | 二氧化硅与苛性钠溶液反应:SiO2+2OH-=SiO32-+H2O | |
| D. | 澄清石灰水中通入少量CO2的反应:CO2+Ca2++2OH-=CaCO3↓+H2O |
15.在常温下,可用铁制容器存放或用铝槽车运输的溶液是( )
| A. | 稀硫酸 | B. | 稀硝酸 | C. | 浓硝酸 | D. | 硫酸铜溶液 |
12.原子序数依次增大的X、Y、Z、W、R为短周期主族元素,X原子的质子数与电子层数相同,Y和W的原子序数相差8,W原子最外层电子数是最内层电子数的3倍,Y、Z、W三种原子的最外层电子数之和为l5.下列说法正确的是( )
| A. | 简单离子半径:Z>Y | B. | 阳离子的氧化性:X>Z | ||
| C. | 氧化物对应水化物的酸性:R>W | D. | X和Y只能形成一种化合物 |
19.下列关于热化学反应的描述中正确的是( )
| A. | 已知中和热为57.3kJ/mol,则HCl+NaOH═NaCl+H2O△H=-57.3kJ/mol | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)△H=+2×283.0kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
16.下列过程中不一定释放能量的是 ( )(请填编号)
| A. | 形成化学键 | B. | 燃料燃烧 | ||
| C. | 化合反应 | D. | 葡萄糖在体内的氧化分解 | ||
| E. | 酸碱中和 | F. | 炸药爆炸 |
13.下列各组物质,只通过混合后现象无法鉴别的是( )
| A. | HCl、Na2CO3 | B. | AlCl3、NaOH | C. | NaAlO2、HCl | D. | MgCl2、AgNO3 |
15.一定条件下,反应:C(s)+CO2(g)?2CO(g)在2L恒容密闭容器中进行,反应进行20s时,CO的物质的量增加了0.40mol,则下列说法正确的是( )
| A. | 该反应是一熵减反应 | |
| B. | 升高温度时,反应向逆方向进行 | |
| C. | 反应平衡时,v (CO2):v (CO)=1:2 | |
| D. | 充入N2使体系压强增大,能提高反应速率 |
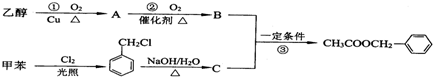
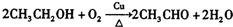 .
. .
.