��Ŀ����
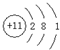
13��������Ԫ��A��B��C��D��E��ԭ��������������AԪ�������ӵ�ԭ�Ӻ���û�е��ӣ�B�ǿ����к�������Ԫ�أ�CԪ��ԭ������������������Ӳ�����������C��D���γ����ֳ��������ӻ������ҵ�ϳ��õ��C��E�Ļ��������Ʊ�E���ʣ���1������DԪ�ص�ԭ�ӽṹʾ��ͼ
 ��C��D��E�ļ����Ӱ뾶��С�����˳��Al3+��Na+��O2-�� �����ӷ��ű�ʾ����
��C��D��E�ļ����Ӱ뾶��С�����˳��Al3+��Na+��O2-�� �����ӷ��ű�ʾ������2��д��Ԫ��E�����ڱ��е�λ�õ������ڢ�A�壮
��3����ҵ�ϳ���A��B�ĵ��ʺϳ�һ�ֳ������壬������ĵ���ʽ
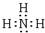 �����������ij��÷���������ʪ�ĺ�ɫʯ����ֽ�ӽ������壬����ֽ������֤���������ڣ�
�����������ij��÷���������ʪ�ĺ�ɫʯ����ֽ�ӽ������壬����ֽ������֤���������ڣ���4��D2C2��H2O��Ӧ�Ļ�ѧ����ʽ��2Na2O2+2H2O=4NaOH+O2����D2C2��CuSO4��Һ��Ӧ�������Dz�����ɫ�����������ݷų���
��5����Ԫ��A��B��C��ԭ�Ӹ�����4��2��3�γɵĻ����д������뷽��ʽ��NH4NO3=NH4++NO3-��
���� ������Ԫ��A��B��C��D��E��ԭ��������������AԪ�������ӵ�ԭ�Ӻ���û�е��ӣ���AΪ��Ԫ�أ�B�ǿ����к�������Ԫ�أ�BΪ��Ԫ�أ�CԪ��ԭ������������������Ӳ�����������Cֻ�ܴ��ڵڶ����ڣ�����������Ϊ6����CΪ��Ԫ�أ���C��D���γ����ֳ��������ӻ������DΪNaԪ�أ���ҵ�ϳ��õ��C��E�Ļ��������Ʊ�E���ʣ�EΪAlԪ�أ��ݴ˽��н��
��� �⣺������Ԫ��A��B��C��D��E��ԭ��������������AԪ�������ӵ�ԭ�Ӻ���û�е��ӣ���AΪ��Ԫ�أ�B�ǿ����к�������Ԫ�أ�BΪ��Ԫ�أ�CԪ��ԭ������������������Ӳ�����������Cֻ�ܴ��ڵڶ����ڣ�����������Ϊ6����CΪ��Ԫ�أ���C��D���γ����ֳ��������ӻ������DΪNaԪ�أ���ҵ�ϳ��õ��C��E�Ļ��������Ʊ�E���ʣ�EΪAlԪ�أ�
��1��Naԭ�Ӻ��������Ϊ11����3�����Ӳ㣬���������Ϊ2��8��1��ԭ�ӽṹʾ��ͼΪ�� ��
��
���Ӳ�ṹ��ͬ�˵����Խ�����Ӱ뾶ԽС����C��D��E�����Ӱ뾶Al3+��Na+��O2-��
�ʴ�Ϊ�� ��Al3+��Na+��O2-��
��Al3+��Na+��O2-��
��2��EΪAlԪ�أ�ԭ������Ϊ13���������ڱ��е������ڢ�A�壬
�ʴ�Ϊ���������ڢ�A�壻
��3����ҵ�ϳ���A��B�ĵ��ʺϳ�һ�ֳ�������ΪNH3�������е�ԭ������ԭ��֮���γ�1�Թ��õ��Ӷԣ�������ĵ���ʽ Ϊ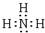 �����鰱���ij��÷����ǣ�����ʪ�ĺ�ɫʯ����ֽ�ӽ������壬����ֽ������֤���������ڣ�
�����鰱���ij��÷����ǣ�����ʪ�ĺ�ɫʯ����ֽ�ӽ������壬����ֽ������֤���������ڣ�
�ʴ�Ϊ��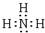 ������ʪ�ĺ�ɫʯ����ֽ�ӽ������壬����ֽ������֤���������ڣ�
������ʪ�ĺ�ɫʯ����ֽ�ӽ������壬����ֽ������֤���������ڣ�
��4��Na2O2��H2O��Ӧ����NaOH��O2����ѧ����ʽ��2Na2O2+2H2O=4NaOH+O2����Na2O2��CuSO4��Һ��Ӧ��������H2O��Ӧ����NaOH��O2��Ȼ��NaOH��CuSO4��Һ��Ӧ����Cu��OH��2���������ǣ�������ɫ�����������ݷų���
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����������ɫ�����������ݷų���
��5����H��N��O��ԭ�Ӹ�����4��2��3�γɵĻ�����ΪNH4NO3������뷽��ʽΪ��NH4NO3=NH4++NO3-��
�ʴ�Ϊ��NH4NO3=NH4++NO3-��
���� ���⿼��ṹ����λ�ù�ϵ����Ŀ�Ѷ��еȣ��ƶ�Ԫ���ǽ���ؼ����漰��������Ų������Ӱ뾶�Ƚϡ�Ԫ�ػ��������ʡ����û�ѧ�����֪ʶ��ע������ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ��

| A�� | ̼�����Ƿ��ͷ۵���Ҫ�ɷ֣���̼������������θ����һ��ҩ�� | |
| B�� | �����Ƶ�ˮ��Һ�׳�ˮ������������ľ�ķ���� | |
| C�� | ��������һ���Գ������ϴ������������ճ����� | |
| D�� | Ϊ�������������Ӫ���ɷ֣����˶�Ӧʳ������Ӫ��ǿ������ʳƷ |
| A�� | ����Ħ���������22.4 L•mol-1 | |
| B�� | 1 mol H2��ռ�����ԼΪ22.4 L | |
| C�� | �ڱ�״���£�1 mol H2O��g���������22.4 L | |
| D�� | �ڱ�״���£�1 mol NH3��CO���������ռ�����ԼΪ22.4 L |
| A�� | CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=+725.76 kJ•mol-1 | |
| B�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=-285.8 kJ•mol-1 | |
| C�� | 2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��g����H=-1 451.52 kJ•mol-1 | |
| D�� | 2H2+O2�T2H2O��H=-285.8 kJ/mol |
| A�� | ֻҪ��һ�ַ�Ӧ��ļ��ܴ���һ��������ļ��ܣ������Ӧ���Ƿ��ȷ�Ӧ | |
| B�� | ֻҪ��һ�ַ�Ӧ��ļ��ܴ���һ��������ļ��ܣ������Ӧ�������ȷ�Ӧ | |
| C�� | ��Ӧ��ļ���֮�ͱ�������ļ���֮�ʹ��Խ�࣬��Ӧ�ų���������Խ�� | |
| D�� | ��Ӧ��ļ���֮�ͱ�������ļ���֮�ʹ��Խ�࣬��Ӧ���յ�������Խ�� |
| A�� | H2 | B�� | Cl2 | C�� | HCl | D�� | O2 |
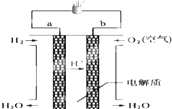 ����Ӧ��ԭ���ԭ�������˶��ֵ�أ������㲻ͬ����Ҫ������ÿС���еĵ�ع㷺ʹ�����ճ���������Ϳ�ѧ�����ȷ��棬����������ṩ����Ϣ����д�ո�
����Ӧ��ԭ���ԭ�������˶��ֵ�أ������㲻ͬ����Ҫ������ÿС���еĵ�ع㷺ʹ�����ճ���������Ϳ�ѧ�����ȷ��棬����������ṩ����Ϣ����д�ո�