题目内容
把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6L H2(标准状况下).试计算:
(1)该合金中铝的质量分数;
(2)该合金中铝和镁的物质的量之比;
(3)若向反应后的溶液中加入足量的NaOH溶液,最终能产生沉淀多少克?
(1)该合金中铝的质量分数;
(2)该合金中铝和镁的物质的量之比;
(3)若向反应后的溶液中加入足量的NaOH溶液,最终能产生沉淀多少克?
考点:有关混合物反应的计算
专题:计算题
分析:根据盐酸过量,则镁、铝都完全反应,根据金属的质量关系和得失电子守恒来列式计算Mg、Al的各自物质的量,根据m=nM计算Al的质量,进而计算Al的质量分数;向反应后的溶液中加入足量的NaOH溶液,最终能产生沉淀为氢氧化镁,根据Mg原子守恒n[Mg(OH)2])=n(Mg),再根据m=nM计算其质量.
解答:
解:标准状况下,氢气的物质的量为
=0.25mol,
因盐酸足量,金属完全反应,设镁、铝的物质的量分别为x mol和y mol,则:
,
解得x=0.1,y=0.1mol,
(1)铝的质量分数为
×100%=52.9%,
答:该合金中铝的质量分数为52.9%;
(2)该合金中镁和铝的物质的量之比为0.1mol:0.1mol=1:1,
答:该合金中镁和铝的物质的量之比为1:1;
(3)向反应后的溶液中加入足量的NaOH溶液,最终能产生沉淀为氢氧化镁,根据Mg原子守恒n[Mg(OH)2])=n(Mg)=0.1mol,故生成沉淀的质量=0.1mol×58g/mol=5.8g,
答:生成沉淀的质量为5.8g.
| 5.6L |
| 22.4L/mol |
因盐酸足量,金属完全反应,设镁、铝的物质的量分别为x mol和y mol,则:
|
解得x=0.1,y=0.1mol,
(1)铝的质量分数为
| 0.1mol×27g/mol |
| 5.1g |
答:该合金中铝的质量分数为52.9%;
(2)该合金中镁和铝的物质的量之比为0.1mol:0.1mol=1:1,
答:该合金中镁和铝的物质的量之比为1:1;
(3)向反应后的溶液中加入足量的NaOH溶液,最终能产生沉淀为氢氧化镁,根据Mg原子守恒n[Mg(OH)2])=n(Mg)=0.1mol,故生成沉淀的质量=0.1mol×58g/mol=5.8g,
答:生成沉淀的质量为5.8g.
点评:本题考查混合物计算、金属与酸的反应,比较基础,也可以利用方程式进行解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法正确的是( )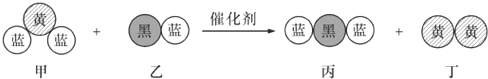

| A、该反应属于置换反应 |
| B、化学方程式中乙、丙的化学计量数均为4 |
| C、甲和丁中同种元素化合价相等 |
| D、甲和丙中所含元素种类相同 |

 某稀硫酸和硝酸的混合溶液200mL,分成两份.向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.
某稀硫酸和硝酸的混合溶液200mL,分成两份.向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO).向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示.