题目内容
将可能混有下列物质的硫酸铵样品13.2g,在加热条件与过量氢氧化钠溶液反应,可收集到气体4.3L (标准状况),则该样品内不可能含有的物质是( )
| A、碳酸氢铵和硝酸铵 |
| B、碳酸铵和硝酸铵 |
| C、氯化铵和碳酸氢铵 |
| D、氯化铵和碳酸铵 |
考点:有关混合物反应的计算
专题:计算题
分析:假设13.2故全部为硫酸铵,其物质的量为
=0.1mol,根据N元素守恒可知生成氨气为0.2mol,标况下氨气的体积为0.2mol×22.4L/mol=4.48L>4.3L,故杂质中铵根离子的含量小于硫酸铵,再结合选项判断.
| 13.2g |
| 132g/mol |
解答:
解:假设13.2故全部为硫酸铵,其物质的量为
=0.1mol,根据N元素守恒可知生成氨气为0.2mol,标况下氨气的体积为0.2mol×22.4L/mol=4.48L>4.3L,故杂质中铵根离子的含量小于硫酸铵,硫酸铵中m(NH4+):m(SO42-)=18:48,
A.碳酸氢铵中m(NH4+):m(HCO3-)=18:61,硝酸铵中m(NH4+):m(NO3-)=18:62,则混合物中铵根离子含量小于硫酸铵,可能含有,故A不选;
B.碳酸铵中m(NH4+):m(CO32-)=18:30,硝酸铵中m(NH4+):m(NO3-)=18:62,则混合物中铵根离子含量可能小于硫酸铵,可能含有,故B不选;
C.氯化铵中m(NH4+):m(Cl-)=18:35.5,碳酸氢铵中m(NH4+):m(HCO3-)=18:61,则混合物中铵根离子含量可能小于硫酸铵,可能含有,故C不选;
D.氯化铵中m(NH4+):m(Cl-)=18:35.5,碳酸铵中m(NH4+):m(CO32-)=18:30,则混合物中铵根离子含量一定大于硫酸铵,不可能含有,故D选,
故选D.
| 13.2g |
| 132g/mol |
A.碳酸氢铵中m(NH4+):m(HCO3-)=18:61,硝酸铵中m(NH4+):m(NO3-)=18:62,则混合物中铵根离子含量小于硫酸铵,可能含有,故A不选;
B.碳酸铵中m(NH4+):m(CO32-)=18:30,硝酸铵中m(NH4+):m(NO3-)=18:62,则混合物中铵根离子含量可能小于硫酸铵,可能含有,故B不选;
C.氯化铵中m(NH4+):m(Cl-)=18:35.5,碳酸氢铵中m(NH4+):m(HCO3-)=18:61,则混合物中铵根离子含量可能小于硫酸铵,可能含有,故C不选;
D.氯化铵中m(NH4+):m(Cl-)=18:35.5,碳酸铵中m(NH4+):m(CO32-)=18:30,则混合物中铵根离子含量一定大于硫酸铵,不可能含有,故D选,
故选D.
点评:本题考查混合物计算,难度中等,注意利用假设法进行解答,注意对化学式中元素或原子团质量分数的理解与灵活应用.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A、标准状况下,22.4LH2中含中子数为2NA |
| B、常温常压下,氧气和臭氧的混合物16g中约含有NA个氧原子 |
| C、电解食盐水若产生2 g氢气,则转移的电子数目为2NA |
| D、100mL 0.1mol?L-1的FeCl3溶液中含有Fe3+的个数为0.01NA |
下列各组物质中,互称为同位素的是( )
| A、126C和146C |
| B、氧气和臭氧 |
| C、纯碱和烧碱 |
| D、生石灰和石灰石 |
今有150ml 1mol/L的烧碱溶液,吸收了2.24LCO2(标准状况),下列有关离子数的说法正确的是( )
| A、HCO3-等于CO32- |
| B、HCO3-略多于CO32- |
| C、HCO3-略少于CO32- |
| D、Na+等于HCO3-与CO32-之和 |
钠-钾合金可在核反应堆中用作热交换液.5.05g钠-钾合金溶于200mL水生成0.075mol氢气.
(1)计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化).
(2)计算并确定该钠-钾合金的化学式.
(1)计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化).
(2)计算并确定该钠-钾合金的化学式.
下列各组有机物中,不论二者以什么比例混合,只要总质量一定,则完全燃烧时消耗O2的质量和生成水的质量不变的是( )
| A、CH4 C2H6 |
| B、C2H6 C3H6 |
| C、C2H4 C3H6 |
| D、C3H4 C3H6 |
化学与人类生活、社会可持续发展密切相关.下列说法正确的是( )
| A、大量使用化肥和农药,以提高农作物产量 |
| B、用CO2合成聚碳酸醋可降解塑料,实现“碳“的循环利用 |
| C、“天宫一号“使用的碳纤维,是一种新型有机高分子材料 |
| D、为改善食品的色、香、味并防止变质,可加入大量食品添加剂 |
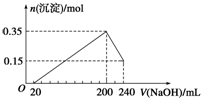 Ⅰ.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成;请填空:
Ⅰ.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成;请填空: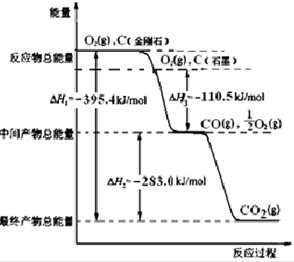 能源危机是当前全球问题,开源节流是应对能源危机的重要举措.
能源危机是当前全球问题,开源节流是应对能源危机的重要举措.