题目内容
已知:①A是石油分解的主要成分,A的产量通常用来衡量一个国家的石油化工水平;
②2CH3CHO+O2
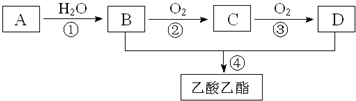
2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
回答下列问题:
(1)写出A的结构式 ;C的结构简式 ;
(2)B、D分子中的官能团分别是 、 .
(3)写出下列反应的反应类型:① ,② ,④ .
(4)写出下列反应的化学方程式:① ;② ;④ .
②2CH3CHO+O2
| 催化剂 |
| △ |

回答下列问题:
(1)写出A的结构式
(2)B、D分子中的官能团分别是
(3)写出下列反应的反应类型:①
(4)写出下列反应的化学方程式:①
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应得到B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步发生氧化反应得到D为CH3COOH,乙醇与乙酸发生酯化反应得到CH3COOCH2CH3,据此解答.
解答:
解:A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应得到B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步发生氧化反应得到D为CH3COOH,乙醇与乙酸发生酯化反应得到CH3COOCH2CH3,
(1)A为乙烯,结构式为 ,C的结构简式为CH3CHO,故答案为:
,C的结构简式为CH3CHO,故答案为: ;CH3CHO;
;CH3CHO;
(2)B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为:羟基;羧基;
(3)反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇被氧化物乙醛,反应④是乙酸与乙醇发生酯化反应生成乙酸乙酯,也属于取代反应,故答案为:加成反应;氧化反应;酯化反应或取代反应;
(4)反应①的化学方程式为:CH2=CH2+H2O
CH3CH2OH;
反应②的化学方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O;
反应④的化学方程式为:CH3COOH+HOC2H5
CH3COOC2H5+H2O,
故答案为:CH2=CH2+H2O
CH3CH2OH;2CH3CH2OH+O2
2CH3CHO+2H2O;CH3COOH+HOC2H5
CH3COOC2H5+H2O.
(1)A为乙烯,结构式为
 ,C的结构简式为CH3CHO,故答案为:
,C的结构简式为CH3CHO,故答案为: ;CH3CHO;
;CH3CHO;(2)B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为:羟基;羧基;
(3)反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇被氧化物乙醛,反应④是乙酸与乙醇发生酯化反应生成乙酸乙酯,也属于取代反应,故答案为:加成反应;氧化反应;酯化反应或取代反应;
(4)反应①的化学方程式为:CH2=CH2+H2O
| 催化剂 |
反应②的化学方程式为:2CH3CH2OH+O2
| Cu |
| △ |
反应④的化学方程式为:CH3COOH+HOC2H5
| 浓硫酸 |
| △ |
故答案为:CH2=CH2+H2O
| 催化剂 |
| Cu |
| △ |
| 浓硫酸 |
| △ |
点评:本题考查有机物推断,涉及烯烃、醇、醛、羧酸之间的转化关系等,难度不大,注意基础知识的理解掌握.

练习册系列答案
相关题目
下列与化学反应能量变化相关的叙述正确的是( )
| A、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
| B、相同条件下2mol氢原子所具有的能量小于1 mol氢分子所具有的能量 |
| C、应用盖斯定律,可以计算某些难以直接测量的反应焓变 |
| D、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行:则该反应的△H>0 |
下列各溶液中,微粒的物质的量浓度关系或说法不正确的是( )
| A、0.1mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| B、0.1mol/L NH4Cl溶液:c(NH4+)<c(Cl-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、常温下物质的量浓度相等①NH4HSO4、②(NH4)2SO4、③(NH4)2CO3三种溶液中c(NH4+):①<②<③ |
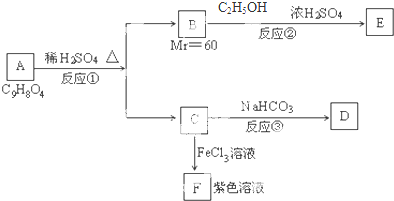 有机物A可发生如下转化:
有机物A可发生如下转化: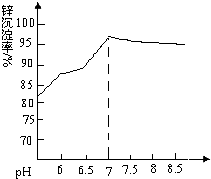 纳米氧化锌是一种新型高功能精细无机产品,由粗氧化锌(含杂质Al2O3、FeO、Fe2O3、CuO等)制备纳米氧化锌.流程依次涉及的部分离子方程式:①FeO+2H+=Fe2++H2O ②H2O2+2Fe2++2H+=2Fe3++2H2O ③Zn+Cu2+=Zn2++Cu
纳米氧化锌是一种新型高功能精细无机产品,由粗氧化锌(含杂质Al2O3、FeO、Fe2O3、CuO等)制备纳米氧化锌.流程依次涉及的部分离子方程式:①FeO+2H+=Fe2++H2O ②H2O2+2Fe2++2H+=2Fe3++2H2O ③Zn+Cu2+=Zn2++Cu

 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如下图所示:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如下图所示: