题目内容
14.在10L恒容密闭容器中发生反应:X(g)+Y(g)?2Z(g)△H<0.T℃时,各物质的物质的量与时间关系如下表:下列说法正确的是( )| 时间/min | n(X)/mol | n(Y)/mol | n(Z)/mol |
| 0 | 0.20 | 0.60 | 0 |
| 10 | a1 | a2 | 0.25 |
| 13 | b1 | 0.45 | b2 |
| 15 | d1 | d2 | 0.30 |
| A. | 前10 min内的平均反应速率v(Y)=2.5×10-3 mol/(L•min) | |
| B. | 保持其它条件不变,升高温度,反应达平衡时c(X)<5.0×10-3 mol/L | |
| C. | 若起始时只充入0.60 mol Z(g),反应达平衡时Z(g)的转化率为50% | |
| D. | 若起始时充入0.60 mol X(g)、0.10 mol Y(g)和0.50 mol Z(g),达到平衡前v(正)>v(逆) |
分析 A.根据v=$\frac{△c}{△t}$计算v(Z),再利用速率之比等于其化学计量数之比计算v(Y);
B.13min时Y的物质的量变化量为0.6mol-0.45mol=0.15mol,则Z的物质的量变化为0.15mol×2=0.3mol,即13min时Z为0.3mol,而15min时Z的物质的量也为0.3mol,故13min时反应到达平衡,根据方程式计算参加反应X物质的量,进而计算平衡时X的浓度,正反应为放热反应,保持其它条件不变,升高温度,平衡向逆反应方向移动;
C.由于反应前后气体化学计量数相等,利用物质的量代替浓度代入K=$\frac{{c}^{2}(Z)}{c(X)×c(Y)}$计算平衡常数,设到达平衡时参加反应Z为n mol,用三段式表示出平衡时各组分物质的量,再根据平衡常数列方程计算n的值,进而计算Z的转化率;
D.计算此时浓度商Qc,与平衡常数比较,判断反应进行方向,进而判断达到平衡前v(正)、v(逆)的相对大小.
解答 解:A.前10 min内Z的物质的量变化量为0.25mol,容器体积为10L,则v(Z)=$\frac{\frac{0.25mol}{10L}}{10min}$=0.0025mol/(L.min)=,速率之比等于其化学计量数之比,则v(Y)=$\frac{1}{2}$v(Z)=$\frac{1}{2}$×0.0025mol/(L.min)=v(Z)=0.00125mol/(L.min),故A错误;
B.13min时Y的物质的量变化量为0.6mol-0.45mol=0.15mol,则Z的物质的量变化为0.15mol×2=0.3mol,即13min时Z的物质的量为b2=0.3mol,而15min时Z的物质的量也为0.3mol,故13min时反应到达平衡,由X(g)+Y(g)?2Z(g),可知参加反应X为0.15mol,故平衡时X的物质的量b1=0.2mol-0.15mol=0.05mol,故平衡时c(X)=$\frac{0.05mol}{10L}$=5.0×10-3 mol/L,正反应为放热反应,保持其它条件不变,升高温度,平衡向逆反应方向移动,X的浓度增大,即反应达平衡时c(X)>5.0×10-3 mol/L,故B错误;
C.由B中计算可知,平衡时X、Y、Z的物质的量分别为0.05mol、0.45mol、0.3mol,由于反应前后气体化学计量数相等,利用物质的量代替浓度计算平衡常数,故平衡常数K=$\frac{{c}^{2}(Z)}{c(X)×c(Y)}$=$\frac{0.{3}^{2}}{0.05×0.45}$=4,
设到达平衡时参加反应Z为n mol,则:
X(g)+Y(g)?2Z(g)
开始(mol):0 0 0.6
转化(mol):0.5n 0.5n n
平衡(mol):0.5n 0.5n 0.6-n
则$\frac{(0.6-n)^{2}}{0.5n×0.5n}$=4,解得n=0.3,故Z的转化率为$\frac{0.3mol}{0.6mol}$×100%=50%,故C正确;
D.此时浓度商Qc=$\frac{0.{5}^{2}}{0.6×0.1}$=$\frac{25}{6}$>K=1,故反应向逆反应方向进行,则v(正)<v(逆),故D错误,
故选:C.
点评 本题考查化学平衡计算、化学平衡常数计算及应用,关键根据表中数据计算判断13min处于平衡状态,注意对平衡常数的理解与灵活应用,难度中等.

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案| A. | a-lg2 | B. | b-lg2 | C. | a+lg2 | D. | b+lg2 |
 某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验.
某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验.实验1:铜与浓硫酸反应,实验装置如图所示.
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面;
(1)能够证明铜与浓硫酸反应产生的气体的现象:B中品红溶液褪色.
(2)在盛有氯化钡溶液的C试管中除了导管口有气泡外,无其他明显现象,若将其分为两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应位置.
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | BaSO4 | BaSO3 |
(3)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是:当A中气体压强减小时,外界大气压不变,空气从E进入A,使A中压强平衡.
(4)将SO2气体通入含有n mol Na2S溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体2.5nmol. (不考虑溶解的SO2).
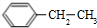 (g)?
(g)?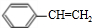 (g)+H2(g)△H=a kJ•mol-1.经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
(g)+H2(g)△H=a kJ•mol-1.经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A. | 反应在前20 min的平均速率为v(H2)=0.004mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol•L-1,则a<0 | |
| C. | 保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0% | |
| D. | 相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v(正)>v(逆) |
| A. | a+8-m-n | B. | a+16-m-n | C. | a-8-(m+n) | D. | a-(m+n) |
①甲跟水反应比乙与水反应剧烈
②甲单质能从乙的盐溶液中置换出单质乙
③甲的最高价氧化物的水化物碱性比乙的最高价氧化物的水化物碱性强
④与某非金属反应时甲原子失电子数目比乙的多
⑤以甲、乙金属为电极构成原电池,甲作负极.
| A. | ①④ | B. | ③⑤ | C. | ①②③④⑤ | D. | ①②③⑤ |
| A. |  | B. | 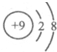 | C. | 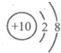 | D. | 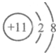 |
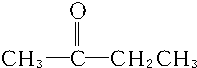 C:CH2═CH-CH2CH3或CH3CH═CH-CH3.
C:CH2═CH-CH2CH3或CH3CH═CH-CH3.