题目内容
1.有如图所示的电化学装置(盐桥内是饱和KNO3、琼脂)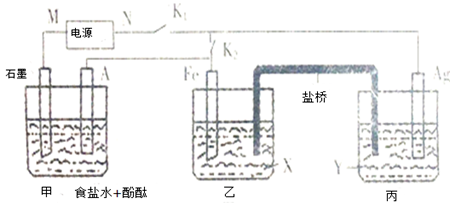
I关闭K1,断开K2,当Y 是AgNO3、X是Fe(NO3)2,通电到5min时,银电极增重2.16g.
(1)N是阳极,此时若将甲烧杯中溶液混合均匀,则溶液的pH=12(食盐水的体积为2L)
(2)前5min内石墨电极上的电极反应式为2H++2e-=H2↑,此阶段内,丙中阳离子浓度变化情况为减小.(填“增大”“减小”或“不变”)
(3)5min时停止通电,将甲、乙装置中的溶液全部混合在一起,从理论上讲,得到的沉淀最多是1.8g.
II关闭K2、断开K1后,若电化学装置中的总反应式为Fe+2Ag+=Fe2++2Ag
(4)X、Y应该分别为A (填序号)
A.Fe(NO3)2、AgNO3
B.FeC12、AgNO3
C.AgNO3、Fe(NO3)2.
分析 关闭K1,断开K2,乙和丙构成原电池,甲是电解池,Fe是负极,Ag是正极,银电极发生反应:Ag++e-=Ag,银电极增重2.16g,即析出金属银0.02mol,转移电子是0.02mol,
(1)Ag是正极,N是阳极,根据电极反应:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-,结合电子转移进行计算;
(2)石墨电极是阴极,发生还原反应,在原电池的正极上发生还原反应;
(3)根据电解原理,甲装置产生氢氧化钠,乙装置发生电极反应Fe-2e-=Fe2+,将甲、乙装置中的溶液全部混合在一起,亚铁离子和氢氧根离子之间反应生成氢氧化亚铁沉淀;
(4)根据盐桥原电池的构成特点,金属铁应该插入含有亚铁离子的盐溶液中,金属银插入含有银离子的盐溶液中.
解答 解:关闭K1,断开K2,乙和丙构成原电池,甲是电解池,Fe是负极,Ag是正极,银电极发生反应:Ag++e-=Ag,银电极增重2.16g,即析出金属银0.02mol,转移电子是0.02mol,
(1)Ag是正极,N是阳极,根据电极反应:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-,转移电子0.02mol,所以生成氢氧化钠物质的量是0.02mol,所以c(NaOH)=$\frac{0.02mol}{2L}$=0.01mol/L,所以pH=12,故答案为:阳;12;
(2)石墨电极是阴极,发生反应:2H++2e-=H2↑,丙中发生反应:Ag++e-=Ag,阳离子浓度减小,故答案为:2H++2e-=H2↑;减小;
(3)5min时停止通电,将甲、乙装置中的溶液全部混合在一起,甲装置产生氢氧化钠是0.02mol,乙装置发生电极反应Fe-2e-=Fe2+,转移电子0.02mol,生成亚铁离子是0.02mol,将甲、乙装置中的溶液全部混合在一起,亚铁离子和氢氧根离子之间反应生成氢氧化亚铁沉淀,从理论上讲,得到的沉淀是氢氧化亚铁0.02mol,质量是0.02mol×90g/mol=1.8g,故答案为:1.8;
(4)根据盐桥原电池的构成特点,金属铁应该插入含有亚铁离子的盐溶液中,金属银插入含有银离子的盐溶液中,所以X、Y应该分别为Fe(NO3)2,AgNO3.
故选A.
点评 本题考查学生电解池和原电池的工作原理以及电极反应式的书写和计算知识,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案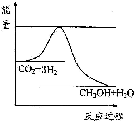 以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ/mol
①该反应在高温下能自发进行的原因是△S>0
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是BDF(填字母,下同).
A.容器中的压强不变 B.1mol H-H 键断裂的同时断裂2mol H-O 键
C.V (CO)=V (H2)D.密闭容器的容积不再改变
E.消耗1mol 水的同时生成1mol H2 F.容器的密度不变
③该反应的平衡常数的表达式K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$.
(2)水煤气再进一步反应可制取氢气.反应为H2O(g)+CO(g)?H2(g)+CO2(g),某温
度下该反应的逆反应平衡常数K=$\frac{4}{9}$.该温度下在甲、乙、丙三个恒容密闭容器中,只
投入H2(g)和CO2(g),其起始浓度如下表所示.下列判断不正确的是B.
| 起始 浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
B.平衡时,甲中和丙中H2的转化率不等
C.平衡时,丙中c(CO2)是甲中的2 倍
D.平衡时,乙中CO2的转化率大于60%
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.在体积为1L 的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c (CH3OH)减小的是A.
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来 D.再充入1mol CO2 和3mol H2.
| A. | 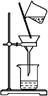 除去粗盐溶液中的不溶物 | B. |  碳酸氢钠受热分解 | ||
| C. | 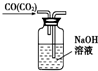 除去CO气体中的CO2气体 | D. | 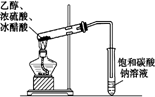 乙酸乙酯制备演示实验 |
 某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:
某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:已知①A、B、C、D、G含有同种元素.
②
| 纯A(单质) | B溶液 | D固体 | G溶液 | |
| 颜色 | 银白色 | 棕黄色 | 红棕色 | 浅绿色 |
依据以上信息填空:
(1)写出D的化学式:Fe2O3.
(2)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色,写出该变化的化学方程式FeSO4+NaOH=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(3)写出反应A转化为B的化学方程式:2Fe+3Cl2=2FeCl3.
(4)B→F的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.如何检验该反应生成的金属阳离子,简述操作方法及现象取反应后溶液少量滴入酸性高锰酸钾,若紫红色褪去,或滴入铁氰化钾生成蓝色沉淀即证明生成Fe2+离子.

I:(1)第三周期元素M的电离能情况如甲图A所示.则M元素的价层电子排布式是3s2
(2)图B折线c(选填“a”、“b”或“c”)可以表达出第ⅣA族元素氢化物的沸点的变化规律.其中点A表示的分子的化学式为H2O,其沸点较高是因为水分子间可以形成氢键.
(3)COCl2 俗称光气,分子中C原子采取sp2杂化成键;其中分子中的共价键含有C(填序号):
A 2个σ键 1个π键 B 2个键π C 3个σ键、1个π键
Ⅱ:海水中富含氯元素.
(4)KCl广泛应用于医药和农业,KCl晶体中基态的Cl-电子排布式为1s22s22p63s23p6
(5)下列是IA族的Li、Na、K三种金属元素的电离能
| X | Y | Z | |
| 第一电离能(KJ/mol) | 526.2 | 502.8 | 425.2 |
(6)RCl用作有机机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M 三个电子层,它与Cl-形成的晶体结构如图乙所示.R的元素符号是Cu,每个Cl-周围最近的Cl-12个.已知该晶体密度为1.15 g/cm3,则晶胞中最近的R+和Cl-之间的距离为$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{4×99.5}{1.15×6.02×1{0}^{23}}}$cm(NA=6.02×1023/mol,只写出计算表达式即可)
| A. | 0.6mol/L | B. | 1mol/L | C. | 1.2mol/L | D. | 0.5mol/L |
 醋酸是日常生活中常见的弱酸.
醋酸是日常生活中常见的弱酸.