题目内容
16.下列与叙述不正确的是( )| A. | 水蒸气变为液态水时,焓变△H<0 | |
| B. | 对于△H<0的反应,反应物的总焓大于生成物的总焓 | |
| C. | 需要持续加热才能进行的反应△H一定大于0 | |
| D. | Ba(OH)2•8H2O和NH4Cl固体反应,反应物的总键能小于生成物的总键能 |
分析 A、水蒸气变为液态水要放热;
B、△H=生成物能量和-反应物能量和;
C、需要持续加热才能进行的反应为吸热反应;
D、Ba(OH)2•8H2O和NH4Cl固体反应为吸热反应.
解答 解:A、水蒸气变为液态水要放热,所以焓变△H<0,故A正确;
B、△H=生成物能量和-反应物能量和,所以当反应物的总焓大于生成物的总焓时,反应放热,△H<0,故B正确;
C、需要持续加热才能进行的反应为吸热反应,所以△H一定大于0,故C正确;
D、Ba(OH)2•8H2O和NH4Cl固体反应为吸热反应,则反应物的总键能大于生成物的总键能,故D错误;
故选:D.
点评 本题考查了化学反应中的能量变化原因以及形式和求算,题目难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
6.进入秋冬季节后,雾霾这种环境污染问题逐渐凸显.从物质分类来看雾霾属于胶体,它区别于溶液等其它分散系的本质特征是( )
| A. | 胶体粒子不能穿过半透膜,但能通过滤纸空隙 | |
| B. | 胶体粒子带电荷并且在一定条件下能稳定存在 | |
| C. | 胶体的分散质粒子直径在1nm~100nm之间 | |
| D. | 胶体能够产生丁达尔效应 |
7.将等物质的量的A、B混合于2L密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),经5min后测得D的浓度为0.5mol•L-1,c(A):c(B)=3:5,用C的浓度变化表示的平均反应速率为0.1mol•L-1•min-1.下列有关结论正确的是( )
| A. | x的值为1 | B. | v(B)=0.2mol•L-1•min-1 | ||
| C. | 反应开始前A的物质的量为3mol | D. | 5min时A的浓度为0.2mol•L-1 |
11.对于反应2CO(g)+O2(g)?2CO2(g)△H<0,能增大正反应速率且使平衡正向移动的是( )
| A. | 增大容器的容积 | B. | 升高体系的温度 | C. | 移走部分CO2 | D. | 通入大量O2 |
1.工业上制备纯Si反应的热化学方程式如下:SiCl4(g)+2H2(g)?Si(s)+4HCl(g)△H=+QkJ/mol (Q>0),下列说法正确的是( )
| A. | 若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ | |
| B. | 当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/LNaOH恰好反应 | |
| C. | 达平衡后,减小Si的量,有利于平衡正向移动 | |
| D. | 达平衡后,增大压强,可提高SiCl4的转化率 |
5.利用右图所示的装置进行下列实验,预测的现象和实际相符的是( )
| 选项 | ①中的物质 | ②中的物质 | ③中的物质 | ③中的现象 | 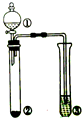 |
| A | 浓氨水 | NaOH | AlCl3溶液 | 先产生白色沉淀,后沉淀溶解 | |
| B | 浓盐酸 | MnO2 | KI溶液 | 溶液变蓝色 | |
| C | 浓硫酸 | Na2SO3 | Ba(NO3)2溶液 | 无沉淀生成 | |
| D | 浓硝酸 | Cu | 含酚酞的NaOH溶液 | 溶液红色褪去 |
| A. | A | B. | B | C. | C | D. | D |
 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出) 