��Ŀ����
����Ŀ����֪��ѧ��Ӧ2C(s)��O2(g)![]() 2CO(g)��2CO(g)��O2(g)
2CO(g)��2CO(g)��O2(g)![]() 2CO2(g)���Ƿ��ȷ�Ӧ���ݴ��ƶ�����ͬ�����£�����˵������ȷ����(����)
2CO2(g)���Ƿ��ȷ�Ӧ���ݴ��ƶ�����ͬ�����£�����˵������ȷ����(����)
A.56 g CO��32 g O2�����е�������֮�ʹ���88 g CO2�����е�������
B.12 g C�����е�����һ������28 g CO�����е�����
C.12 g C��32 g O2���������������44 g CO2�����������
D.������������ȵ�̼��ȫȼ�գ�����CO2�ķ�Ӧ������CO�ķ�Ӧ�ų���������
���𰸡�B
��������
���ݷ��ȷ�Ӧ�з�Ӧ��������������������������������������ȫȼ��ʱ�ų����������ڲ���ȫȼ��ʱ���������ݴ������
A. ��2CO(g)+O2(g)![]() 2CO2(g)�Ƿ��ȷ�Ӧ������56 gCO��32 gO2�����е�����������88 gCO2�����е�������������Ӧ����������������������������A��ȷ��
2CO2(g)�Ƿ��ȷ�Ӧ������56 gCO��32 gO2�����е�����������88 gCO2�����е�������������Ӧ����������������������������A��ȷ��
B. ��2C(s)+O2(g)![]() 2CO(g)�Ƿ��ȷ�Ӧ������12 g C��16 g O2�����е�������һ������28 g CO�����е�������������12g C�����е���������28 g CO�����е�������B����
2CO(g)�Ƿ��ȷ�Ӧ������12 g C��16 g O2�����е�������һ������28 g CO�����е�������������12g C�����е���������28 g CO�����е�������B����
C. ��2C(s)+O2(g)![]() 2CO(g)�� 2CO(g)��O2(g)
2CO(g)�� 2CO(g)��O2(g)![]() 2CO2(g)���Ƿ��ȷ�Ӧ������C+O2
2CO2(g)���Ƿ��ȷ�Ӧ������C+O2![]() CO2Ҳ�Ƿ��ȷ�Ӧ������12 g C��32 g O2�����е�������һ������44 g CO2�����е���������C��ȷ��
CO2Ҳ�Ƿ��ȷ�Ӧ������12 g C��32 g O2�����е�������һ������44 g CO2�����е���������C��ȷ��
D. ��������ȫȼ�շų��������Ȳ���ȫȼ�շų������࣬����һ��������̼ȼ�գ�����CO2������COʱ�ų��������࣬D��ȷ��
�ʺ���ѡ����B��

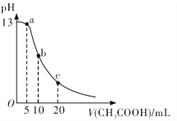
����Ŀ��Ϊ�ⶨһ���ڿ����е�ij�����ữ��FeSO4��Һ��Fe2+�������İٷ��ʣ�ijͬѧȷ��ȡpH=1������Fe2+��Fe3+��ˮ�⣩��FeSO4��Һ200mL���������BaCl2��Һ����ַ�Ӧ����ˡ�ϴ�ӡ�����õ�����28.0g������ȡͬ����FeSO4��Һ200mL�������м������NaOH��Һ������ʹ���ַ�Ӧ��������ȫ����Ϊ���ɫ���ˡ�ϴ�Ӳ��������ù��壬���յù���8.0g��
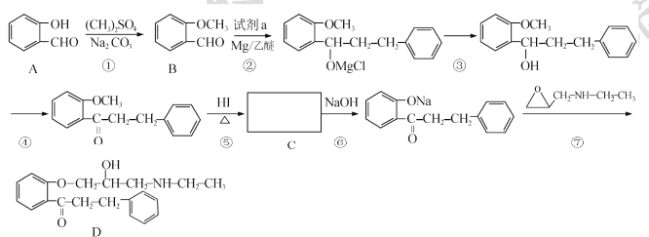
��1��д����Ӧ���漰�Ļ�ѧ����ʽ������3����__��__��__
��2��ͨ�����㣬��д�±���
c��H+�� | c��SO42���� | c��Fe2+��Fe3+�� |
__ | __ | __ |
ע��c��Fe2+��Fe3+����ʾFe2+��Fe3+���ܵ����ʵ�����Ũ��
��3������ԭ��Һ��Fe2+�������İٷ���__��
����Ŀ���ᾧ������������ʧˮʱ�������������FeSO4��7H2O�������������㣬��ֵ�ᳬ��100�������ұ��涨��FeSO4��7H2O�ĺ�����һ��Ʒ99.50����100.5��������Ʒ99.00����100.5��������Ʒ98.00����101.0����
Ϊ�ⶨ��Ʒ��FeSO4��7H2O�������������ɲ�������������������������Һ���еζ���
5Fe2����MnO4����8H����5Fe3����Mn2����4H2O��
2MnO4����5C2O42����16H����2Mn2����10CO2����8H2O
�ⶨ���̣�����һ��Ũ�ȵĸ��������Һ1L��Ȼ���ȡ0.200 g ����Na2C2O4��ʽ��Ϊ134.0��������ƿ�У�������ˮ�ܽⲢ��ϡ�����ữ��������70�桫80�档
(1)��Ҫ�õζ����ⶨ����ĸ��������ҺŨ�ȣ��ζ��յ��������_______________��
(2)����Һ���ȵ�Ŀ����____����Ӧ�տ�ʼʱ��Ӧ���ʽ�С���������¶�����Ӱ���������Ӱ�컯ѧ��Ӧ���ʵ�������������ԭ�������______________________��
(3)���ζ�ʱ���ֵζ��ܼ��첿�������ݣ��ζ�����������ʧ�����ø������Ũ��_____������ƫ������ƫС������Ӱ��������
(4)�ζ���ȥ���������Һ29.50mL����c(KMnO4)��_____mol/L��������λ��Ч���֣���
(5)��ȡ�ķ�FeSO4��7H2O������������Ϊ0.506g�������������������Һ�ζ��ﵽ�յ㣬��¼�ζ�����
�ζ����� ʵ������ | 1 | 2 | 3 | 4 |
V(�������)/mL(������) | 0.10 | 0.20 | 0.00 | 0.20 |
V(�������)/mL(�ն���) | 17.76 | 17.88 | 18.16 | 17.90 |
��������FeSO4��7H2O�ĺ���������������Ϊ_________��С���������λ�������Ϲ���______������
(6)��ʵ��ȷֵΪ99.80%��ʵ��������=____%��������в����Լ����������յ��жϵ�ʧ�����������Ŀ���ԭ���ǣ�__________��