题目内容
【题目】 盐酸普罗帕酮是一种高效速效抗心律失常药。合成此药的原料D的流程如下:
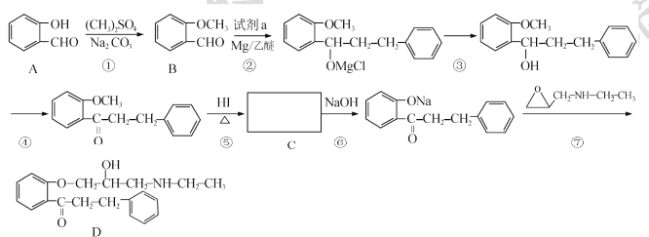
已知: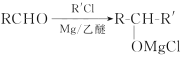
请回答以下问题:
(I)A的化学名称为____,试剂a的结构简式为____。
(2)C的官能团名称为____________。
(3)反应⑤的反应类型为____;反应①和⑤的目的为_______。
(4)满足下列条件的B的同分异构体还有 ___种(不包含B)。其中某同分异构体x能发生水解反应,核磁共振氢谱有4组峰且峰面积比为3:2:2:1,请写出x与NaOH溶液加热反应的化学方程式____。
①能发生银镜反应 ②苯环上有2个取代基
(5)关于物质D的说法,不正确的是____(填标号)。
a.属于芳香族化合物
b.易溶于水
c.有三种官能团
d.可发生取代、加成、氧化反应
【答案】邻羟基苯甲醛(2-羟基苯甲醛) ![]() 羟基,羰基 取代反应 保护羟基不被氧化 11
羟基,羰基 取代反应 保护羟基不被氧化 11 ![]() bc
bc
【解析】
C为 ;
;
(I) 按命名规则给A命名,结合题给信息与反应②中的反应物和产物结构,找出试剂a,可确定结构简式;
(2) 由反应⑤⑥找到C的结构简式,并且找出其的官能团写名称即可;
(3) 找到C的结构简式 是关键,从流程开始的物质A
是关键,从流程开始的物质A 到C
到C ,可发现只有醛基被消除,由此可发现⑤的反应类型及反应①和⑤的目的;
,可发现只有醛基被消除,由此可发现⑤的反应类型及反应①和⑤的目的;
(4)从B的结构![]() 出发,满足条件的B的同分异构体(不包含B)中,先找出条件对应的基团及位置,最后再确定总数目,同分异构体x与NaOH溶液加热下反应,则X含酯基,X核磁共振氢谱有4组峰且峰面积比为3:2:2:1,确定X结构即可求解;
出发,满足条件的B的同分异构体(不包含B)中,先找出条件对应的基团及位置,最后再确定总数目,同分异构体x与NaOH溶液加热下反应,则X含酯基,X核磁共振氢谱有4组峰且峰面积比为3:2:2:1,确定X结构即可求解;
(5) 关于物质D的说法不正确的有哪些?从结构中含有苯环、醚键、羰基、醇羟基等基团的相关概念、性质判断;
(I) A为 ,则其名称为:邻羟基苯甲醛(2-羟基苯甲醛);
,则其名称为:邻羟基苯甲醛(2-羟基苯甲醛);
答案为:邻羟基苯甲醛(2-羟基苯甲醛);
题给信息 ,反应②为
,反应②为 ,则试剂a为
,则试剂a为![]() ;
;
答案为:![]() ;
;
(2) 由反应⑤⑥找到C的结构简式: ,官能团为羟基和羰基;
,官能团为羟基和羰基;
答案为:羟基;羰基;
(3) C的结构简式是 ,
, 与HI在加热下发生反应⑤得到
与HI在加热下发生反应⑤得到 ,可见是-OCH3中的-CH3被H取代了;从流程开始的物质A
,可见是-OCH3中的-CH3被H取代了;从流程开始的物质A 到C
到C ,为什么不采用以下途径:
,为什么不采用以下途径: 主要是步骤3中醇羟基被氧化成羰基时,酚羟基也会被氧化,因此反应①和⑤的目的为保护羟基不被氧化;
主要是步骤3中醇羟基被氧化成羰基时,酚羟基也会被氧化,因此反应①和⑤的目的为保护羟基不被氧化;
答案为:取代反应;保护羟基不被氧化;
(4)B的同分异构体(不包含B)要满足条件 ①能发生银镜反应②苯环上有2个取代基,其中有一个醛基(含甲酸酯基),且取代基可以是邻、间、对3种位置,则2个取代基可以有四种组合:首先是![]() 和
和![]() ,它们分别处于间、对,共2种(处于邻位就是B要排除),剩下3种组合分别是
,它们分别处于间、对,共2种(处于邻位就是B要排除),剩下3种组合分别是![]() 、
、![]() 、
、![]() ,它们都可以是邻、间、对3种位置,就9种,合起来共11种;
,它们都可以是邻、间、对3种位置,就9种,合起来共11种;
答案为:11;
某同分异构体x能与NaOH溶液加热下反应,则X含甲酸酯基,则X中苯环上的侧链为![]() ,X核磁共振氢谱有4组峰且峰面积比为3:2:2:1,则取代基处于对位,因此X为
,X核磁共振氢谱有4组峰且峰面积比为3:2:2:1,则取代基处于对位,因此X为![]() ,则反应方程式为
,则反应方程式为![]() ;
;
答案为:![]()
(5) D为 ,关于物质D的说法:
,关于物质D的说法:
a.因为含有苯环,属于芳香族化合物,a说法正确,不符合;
b.亲水基团少,憎水基团大,不易溶于水,b说法不正确,符合;
c.含氧官能团有3种,还有1种含氮官能团,c说法不正确,符合;
d.醇羟基可发生取代、氧化,羰基、苯环上可催化加氢反应,d说法正确,不符合;
答案为:bc。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D
【题目】依据题目要求回答下列问题。
(1)常温下,浓度均为0.1 mol/L的下列六种溶液的pH如表所示。
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
①上述盐溶液中的阴离子结合H+能力最强的是________。
②根据表中数据,浓度均为0.01 mol/L的下列五种物质的溶液中,酸性最强的是________(填字母编号,下同);将各溶液分别稀释100倍,pH变化最小的是________。
a. HCN b.HClO c. C6H5OH d. CH3COOH e. H2CO3
③下列关于NaHCO3饱和溶液的表述,正确的是________
A. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. c(Na+)+c(H+)=c(HCO3-)+c(OH-)
C.HCO3-的电离程度大于HCO3-的水解程度
④根据上表数据,请你判断下列反应不能成立的是________。
a. CH3COOH+Na2CO3=NaHCO3+CH3COONa
b. CH3COOH+NaCN=CH3COONa+HCN
c. CO2+H2O+NaClO=NaHCO3+HClO
d. CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
⑤要增大氯水中![]() 的浓度,可向氯水中加入少量的碳酸氢钠溶液,写出Cl2与HCO3-反应的离子方程式为________。
的浓度,可向氯水中加入少量的碳酸氢钠溶液,写出Cl2与HCO3-反应的离子方程式为________。
(2)依据表中数据计算CH3COOH的电离常数Ka=________(已知100.4=2.5,用科学计数法表示)