题目内容
3.有A、B、C、D四种短周期元素.已知一个B原子核的原子受到α粒子的轰击得到一个A原子的原子核和一个C原子的原子核,又知C、D元素同主族,且能发生下面两个反应,如下:A、B化合物+B、C化合物$\stackrel{物质的量2:1}{→}$B单质+A、C化合物
A、D化合物+D、C化合物$\stackrel{物质的量2:1}{→}$D单质+A、C化合物
请完成下列问题.
(1)比较B、C原子半径大小;画出D离子的结构示意图.
(2)分别写出上述两个反应方程式.
分析 有A、B、C、D四种短周期元素,一个B原子核的原子受到α粒子的轰击得到一个A原子的原子核和一个C原子的原子核,又知C、D元素同主族,且能发生下面两个反应,如下:
A、B化合物+B、C化合物$\stackrel{物质的量2:1}{→}$B单质+A、C化合物
A、D化合物+D、C化合物$\stackrel{物质的量2:1}{→}$D单质+A、C化合物,
α粒子即氦核,A与C的原子序数的和等于B的原子序数加上2,从给出的两个反应中我们看出,这两个反应都是氧化还原反应中的归中反应,B、D都为具有可变价态的非金属元素,再结合C与D同族,两个反应物的物质的量之比为2:1等条件,在短周期中这样的例子是2H2S+SO2═3S↓+2H2O,A为H,C为O,D为S,B为N元素,
(1)B、C分别是N、O元素,同一周期元素,原子半径随着原子序数增大而减小;D是S元素,硫离子核外有18个电子、核内有16个质子;
(2)AB形成的化合物是氨气、BC形成的化合物是氮氧化物,氨气和氮氧化物反应生成氮气和水,根据转移电子守恒确定氮氧化物成分;
AD形成的化合物是硫化氢、CD形成的化合物是二氧化硫,二者反应生成硫和水.
解答 解:有A、B、C、D四种短周期元素,一个B原子核的原子受到α粒子的轰击得到一个A原子的原子核和一个C原子的原子核,又知C、D元素同主族,且能发生下面两个反应,如下:
A、B化合物+B、C化合物$\stackrel{物质的量2:1}{→}$B单质+A、C化合物
A、D化合物+D、C化合物$\stackrel{物质的量2:1}{→}$D单质+A、C化合物,
α粒子即氦核,A与C的原子序数的和等于B的原子序数加上2,从给出的两个反应中我们看出,这两个反应都是氧化还原反应中的归中反应,B、D都为具有可变价态的非金属元素,再结合C与D同族,两个反应物的物质的量之比为2:1等条件,在短周期中这样的例子是2H2S+SO2═3S↓+2H2O,A为H,C为O,D为S,B为N元素,
(1)B、C分别是N、O元素,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径N>O,即B>C;D是S元素,硫离子核外有18个电子、核内有16个质子,其离子结构示意图为 ,
,
故答案为:B>C; ;
;
(2)AB形成的化合物是氨气、BC形成的化合物是氮氧化物,氨气和氮氧化物反应生成氮气和水,根据转移电子守恒确定氮氧化物成分为,所以该反应方程式为2NH3+N2O3═2N2+3H2O;
AD形成的化合物是硫化氢、CD形成的化合物是二氧化硫,二者反应生成硫和水,反应方程式为2H2S+SO2═3S↓+2H2O,故答案为:2NH3+N2O3═2N2+3H2O;2H2S+SO2═3S↓+2H2O.
点评 本题考查原子结构和元素周期律,为高频考点,侧重考查学生分析推断能力,明确原子结构、元素周期表结构及物质性质是解本题关键,熟悉常见元素化合物性质,题目难度不大.

 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案| A. | 2g | B. | 3g | C. | 3.5g | D. | 4.5g |
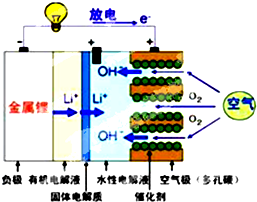 美国IBM公司设计出了一款新型锂空气电池,其原理就是通过吸入空气与设备内的锂离子发生反应,进行能量的提供.因其独特的放电方式,也称呼吸式电池.负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液.中间设有用于隔开正极和负极的锂离子固体电解质.正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合.如图所示.下列说法不正确的是( )
美国IBM公司设计出了一款新型锂空气电池,其原理就是通过吸入空气与设备内的锂离子发生反应,进行能量的提供.因其独特的放电方式,也称呼吸式电池.负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液.中间设有用于隔开正极和负极的锂离子固体电解质.正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合.如图所示.下列说法不正确的是( )| A. | 负极反应:Li-e-=Li+,金属锂以锂离子(Li+)的形 式溶于有机电解液,电子供应给导线.溶解的锂离子(Li+)穿过固体电解质移到正极的水性电解液中 | |
| B. | 正极反应:O2+2H2O+4e-=4OH-,在正极的水性电解液中与锂离子(Li+)结合生成水溶性氢氧化锂(LiOH),并能实现锂元素的循环 | |
| C. | 在负极的有机电解液和空气极的水性电解液之间,用只能通过锂离子的固体电解质隔开,以防止两电解液发生混合,而且能促进电池发生反应 | |
| D. | 锂-空气电池至今都未普及,原因是它存在致命缺陷,即固体反应生成物氧化锂(Li2O)在正极堆积,使电解液与空气的接触被阻断,从而导致放电停止 |
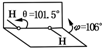 我国科学家卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素(H2NCONH2)和H2O2形成加合物H2NCONH2•H2O2,不但使H2O2稳定下来,而且结构也没有发生改变,得到了可供做衍射实验的单晶体,经测定H2O2结构如图所示,结合以上信息,有关过氧化氢的说法不正确的是( )
我国科学家卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素(H2NCONH2)和H2O2形成加合物H2NCONH2•H2O2,不但使H2O2稳定下来,而且结构也没有发生改变,得到了可供做衍射实验的单晶体,经测定H2O2结构如图所示,结合以上信息,有关过氧化氢的说法不正确的是( )| A. | H2NCONH2与H2O2是通过氢键结合的 | B. | H2O2是极性分子 | ||
| C. | H2O2既有氧化性又有还原性 | D. | H2NCONH2•H2O2属于离子化合物 |
| A. | 1mol Cl2参加反应,转移的电子数一定为2NA | |
| B. | 常温常压下,23g NO2与N2O4的混合气体中氮原子数为0.5NA | |
| C. | 标准状况下,22.4L乙烯中含极性共价键数为4NA | |
| D. | 2L 0.1mol•L-1的HClO溶液中含有的H+离子数小于0.2NA |
| A. | Na+、K+、Cl-、F- | B. | Fe2+、ClO-、NO3-、Na+ | ||
| C. | Fe2+、Mg2+、SO42-、Cl- | D. | CO32-、SO42-、Na+、K+ |
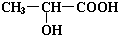 .试回答:
.试回答: +2Na→
+2Na→ +H2↑.
+H2↑.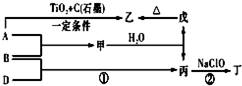 已知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol 丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件巳略去).
已知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol 丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件巳略去).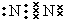 .写出丙的结构式
.写出丙的结构式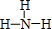 .
.