题目内容
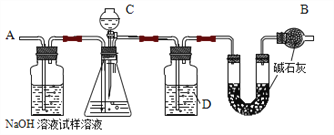
【题目】某纯碱样品中含有氯化钠杂质,用下图装置测定试样中纯碱的纯度。主要实验步骤如下:
①按图组装仪器并检查装置的气密性
②将 a g 样品放入锥形瓶,加适量水溶解。
③称量装有碱石灰的 U 形管的质量为 b g
④从C 滴下溶液到锥形瓶中无气泡产生
⑤从A 处缓缓鼓入一定量空气后,最终称得U 形管的质量为 c g
(1)B 仪器的名称是_____,其作用为_____。
(2)C 中装的溶液是_____(填字母,下同)D 中装的溶液是_____。
a.稀硫酸 b.浓硫酸 c.氢氧化钠溶液 d.浓盐酸
(3)步骤⑤的目的是_____。
(4)写出纯碱的纯度的计算式_____(用字母表示)。
(5)若实验中发现装置 C 的活塞没塞紧,存在漏气情况,则所测得的结果会_____(填“偏大”、“偏小”或“无影响”)。
【答案】 干燥管 防止空气中水汽和二氧化碳进入 U 形管 a b 将产生的二氧化碳赶入 U 形管 纯碱%=[(c-b)/44]×106/a×100% 偏小
【解析】(1)B仪器的名称是干燥管。由于空气中含有水蒸气和二氧化碳,则其作用为防止空气中水蒸汽和二氧化碳进入U形管。(2)浓硫酸溶于水放热,浓盐酸易挥发,氢氧化钠与碳酸钠不反应,所以C中装的溶液是稀硫酸,答案选a;由于生成的二氧化碳中含有水蒸气,碱石灰也吸收水蒸气,则D中装的溶液是浓硫酸,用来干燥生成的二氧化碳。(3)由于装置中会残留剩余的二氧化碳,则步骤⑤的目的是将产生的二氧化碳赶入U形管,减少实验误差。(4)实验前后U形管的质量差就是反应中生成的二氧化碳,质量是(c-b)g,根据碳原子守恒可知纯碱的纯度的计算式为 。(5)若实验中发现装置C的活塞没塞紧,存在漏气情况,二氧化碳会逸出,则所测得的结果会偏小。
。(5)若实验中发现装置C的活塞没塞紧,存在漏气情况,二氧化碳会逸出,则所测得的结果会偏小。

【题目】用如图所示装置制备乙烯的方案正确且检验乙烯时不需要除杂装置X的是![]()

乙烯的制备 | 试剂X | 试剂Y | |
A |
| 水 |
|
B |
| NaOH溶液 |
|
C |
| NaOH溶液 |
|
D |
| 水 |
|
A. A B. B C. C D. D
