题目内容
比较1molN2和1molNO的下列物理量:①质量 ②分子总数 ③原子总数 ④体积,其中一定相等的是( )
| A、① | B、②③ |
| C、①②③ | D、①②③④ |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:根据n=
=
=
结合分子构成以及气体存在的体积计算.
| m |
| M |
| N |
| NA |
| V |
| Vm |
解答:
解:M(N2)=28g/mol,M(NO)=30g/mol,二者摩尔质量不同,则由m=nM可知质量不同,①错误;
二者都是双原子分子,则等物质的量时,分子总数、原子总数相同,则②③正确;
由于气体存在的条件未知,则等物质的量时体积不一定相等,④错误.
故选B.
二者都是双原子分子,则等物质的量时,分子总数、原子总数相同,则②③正确;
由于气体存在的条件未知,则等物质的量时体积不一定相等,④错误.
故选B.
点评:本题考查阿伏伽德罗定律及其推论,为高考高频考点,侧重于学生的分析能力和计算能力的考查,相关计算公式的运用以及气体存在的条件,为易错点,难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、生成物总能量一定低于反应物总能量 |
| B、酒精可用作燃料,说明酒精燃烧是放热反应 |
| C、硝酸铵溶于水温度降低,这个变化是吸热反应 |
| D、同温同压下,H2和Cl2在光照和点燃条件下的△H不同 |
欲配制480mL0.1mol/LCuSO4溶液,正确的方法是( )
| A、称量7.68gCuSO4溶于水中形成480mL溶液 |
| B、称量8.0gCuSO4 溶于500mL水中 |
| C、称量12.5gCuSO4?5H2O溶于水中形成500mL溶液 |
| D、称量12.0gCuSO4?5H2O溶于480mL水中 |
常温时向某溶液中滴入石蕊试液,溶液呈蓝色,其中可能大量共存的离子是( )
| A、Fe3+、Na+、Cl-、SO42- |
| B、S2-、Na+、Cl-、ClO- |
| C、Al3+、K+、SO32-、S2- |
| D、Ag(NH3)2+、K+、Cl-、OH- |
下列各情况,在其中Fe片腐蚀最快的是( )
A、 |
B、 |
C、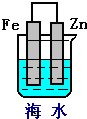 |
D、 |
下列说法正确的是( )
| A、氯离子的半径比氯原子的大 |
| B、氯气和氯离子都有毒 |
| C、氯气和氯离子都呈黄绿色 |
| D、氯气和氯离子都具有氧化性 |
下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据.
根据以上数据分析,下列说法正确的是( )
| 元素 | I1/eV | I2/eV | I3/eV |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A、甲的金属性比乙弱 |
| B、乙的化合价为+1价 |
| C、丙一定为非金属元素 |
| D、丁一定为金属元素 |