题目内容
下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成.请用相应的化学用语回答下列问题:
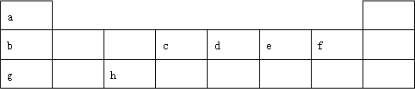
(1)上述标出的8种元素中非金属性最强的是 .(填元素符号)
(2)e元素名称为 .
(3)h的单质能与g元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式 .
(4)g 和e形成的化合物g2e2的电子式为 .
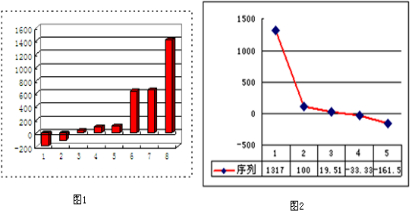
(5)如图1是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则其中柱形“8”代表Si,则其中柱形“2”代表 .(填化学式)
(6)b、c、d、e、f的氢化物的沸点(℃)直角坐标图(如图2),序列“5”的氢化物的化学式是 ,序列“2”的氢化物的结构式为 .

(1)上述标出的8种元素中非金属性最强的是
(2)e元素名称为
(3)h的单质能与g元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式
(4)g 和e形成的化合物g2e2的电子式为

(5)如图1是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则其中柱形“8”代表Si,则其中柱形“2”代表
(6)b、c、d、e、f的氢化物的沸点(℃)直角坐标图(如图2),序列“5”的氢化物的化学式是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表中的位置知,a、b、c、d、e、f、g、h分别是H、Li、C、N、O、F、Na、Al元素,
(1)元素非金属性最强的元素位于周期表右上角;
(2)e元素名称是氧;
(3)g元素最高价氧化物的水化物是NaOH,Al和NaOH溶液反应生成偏铝酸钠和氢气;
(4)g 和e形成的化合物g2e2的为Na2O2,Na2O2中钠离子和过氧根离子之间存在离子键,O原子之间存在共价键;
(5)分子晶体熔点与其相对分子质量成正比,且分子晶体熔点高低还与其状态有关,气体熔点小于固体,原子晶体熔点最高,金属晶体熔点与其原子半径成反比;
(6)b、c、d、e、f分别为Li、C、N、O、F,由氢化物的沸点(℃)直角坐标图可知,5最小为甲烷,2的氢化物是水.
(1)元素非金属性最强的元素位于周期表右上角;
(2)e元素名称是氧;
(3)g元素最高价氧化物的水化物是NaOH,Al和NaOH溶液反应生成偏铝酸钠和氢气;
(4)g 和e形成的化合物g2e2的为Na2O2,Na2O2中钠离子和过氧根离子之间存在离子键,O原子之间存在共价键;
(5)分子晶体熔点与其相对分子质量成正比,且分子晶体熔点高低还与其状态有关,气体熔点小于固体,原子晶体熔点最高,金属晶体熔点与其原子半径成反比;
(6)b、c、d、e、f分别为Li、C、N、O、F,由氢化物的沸点(℃)直角坐标图可知,5最小为甲烷,2的氢化物是水.
解答:
解:根据元素在周期表中的位置知,a、b、c、d、e、f、g、h分别是H、Li、C、N、O、F、Na、Al元素,
(1)元素非金属性最强的元素位于周期表右上角,所以非金属性最强的是F,故答案为:F;
(2)e元素名称是氧,故答案为:氧;
(3)g元素最高价氧化物的水化物是NaOH,Al和NaOH溶液反应生成偏铝酸钠和氢气,离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;
(4)g 和e形成的化合物g2e2的为Na2O2,Na2O2中钠离子和过氧根离子之间存在离子键,O原子之间存在共价键,电子式为 ,故答案为:
,故答案为: ;
;
(5)分子晶体熔点与其相对分子质量成正比,且分子晶体熔点高低还与其状态有关,气体熔点小于固体,原子晶体熔点最高,金属晶体熔点与其原子半径成反比,所以柱形“2”代表氯气,化学式为Cl2,故答案为:Cl2;
(6)b、c、d、e、f分别为Li、C、N、O、F,由氢化物的沸点(℃)直角坐标图可知,5最小为甲烷,而其它物质中LiH为离子晶体,N、O、F对应的氢化物都含有氢键,沸点较高,水常温下是液体,所以2的氢化物是H2O,
故答案为:CH4;H-O-H.
(1)元素非金属性最强的元素位于周期表右上角,所以非金属性最强的是F,故答案为:F;
(2)e元素名称是氧,故答案为:氧;
(3)g元素最高价氧化物的水化物是NaOH,Al和NaOH溶液反应生成偏铝酸钠和氢气,离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;
(4)g 和e形成的化合物g2e2的为Na2O2,Na2O2中钠离子和过氧根离子之间存在离子键,O原子之间存在共价键,电子式为
 ,故答案为:
,故答案为: ;
;(5)分子晶体熔点与其相对分子质量成正比,且分子晶体熔点高低还与其状态有关,气体熔点小于固体,原子晶体熔点最高,金属晶体熔点与其原子半径成反比,所以柱形“2”代表氯气,化学式为Cl2,故答案为:Cl2;
(6)b、c、d、e、f分别为Li、C、N、O、F,由氢化物的沸点(℃)直角坐标图可知,5最小为甲烷,而其它物质中LiH为离子晶体,N、O、F对应的氢化物都含有氢键,沸点较高,水常温下是液体,所以2的氢化物是H2O,
故答案为:CH4;H-O-H.
点评:本题考查元素周期表和元素周期律的综合应用,明确元素位置、元素周期律及其性质即可解答,(4)(5)题为学习难点,注意氢键对物质性质的影响,题目难度不大.

练习册系列答案
相关题目
下列离子检验的方法正确的是( )
| A、某溶液中滴加AgNO3溶液有白色沉淀,说明原溶液中有Cl- |
| B、某溶液中先滴加足量盐酸无现象,再滴加BaCl2溶液有白色沉淀,说明原溶液中有SO42- |
| C、某溶液中滴加NaOH溶液有蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液中滴加稀硫酸生成无色气体,说明原溶液中有CO32- |
下列物质不能暴露在空气中的是( )
| A、金属钠 | B、玻璃 |
| C、陶瓷 | D、氯化钠 |
2011年是国际化学年.中国的宣传口号是“化学--我们的生活.我们的未来”.下列有关叙述不正确的是( )
| A、大量排放SO2、NO2或CO2都会导致酸雨的形成 |
| B、利用太阳能、潮汐能、风力发电,以获取清洁能源 |
| C、采用纳米二氧化钛光触媒技术.将汽车尾气中的NO和CO转化为无害气体 |
| D、在家用燃煤中加人适量的生石灰能有效减少二氧化硫的排放量 |
比较1molN2和1molNO的下列物理量:①质量 ②分子总数 ③原子总数 ④体积,其中一定相等的是( )
| A、① | B、②③ |
| C、①②③ | D、①②③④ |