题目内容
10.燃料电池是一种新型电池,能够把化学能转化为电能.某甲烷氧气燃料电池的基本反应是X极:O2(g)+2H2O+4e-═4OH-;Y极:CH4(g)-8e-+10OH-═CO${\;}_{3}^{2-}$+7H2O.下列判断中正确的是( )| A. | Y极是正极 | B. | X极发生氧化反应 | ||
| C. | 电子由X极经外电路流向Y极 | D. | 此电池的电解质溶液呈碱性 |
分析 原电池中,负极发生氧化反应,正极发生还原反应,电子从负极经外电路流向正极,注意从化合价变化的角度判断.
解答 解:X极:O2(g)+2H2O+4e-═4OH-,该反应中O2得电子被还原,发生还原反应,应为原电池的正极反应,
A、X极是正极,故A错误;
B、Y极:CH4(g)-8e-+10OH-═CO32-+7H2O,Y极发生氧化反应,故B错误;
C、电子由Y极经外电路流向X极,故C错误;
D、Y极:CH4(g)-8e-+10OH-═CO32-+7H2O,所以此电池的电解质溶液呈碱性,故D正确;
故选D.
点评 本题考查电极反应的判断,题目难度不大,解答本题可从化合价的变化的角度入手,把握电极反应.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
20.下列化合物不能由单质和Cl2直接化合制得的是( )
| A. | MgCl2 | B. | CuCl2 | C. | FeCl2 | D. | HCl |
1.下列反应中属于吸热反应的是( )
| A. | 酸与碱发生中和反应 | B. | 木炭的燃烧 | ||
| C. | 生石灰与水作用制成熟石灰 | D. | 用氢气还原氧化铜 |
18.由A、B、C、D四种金属按表中装置图进行实验.
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)装置丙中溶液的pH变大(填“变大”“变小”或“不变”).
(4)四种金属活泼性由强到弱的顺序是D>A>B>C.
(5)A、C形成合金,露置在潮湿空气中,A先被腐蚀.
| 装置 | 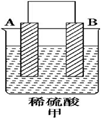 |  | 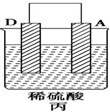 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)装置丙中溶液的pH变大(填“变大”“变小”或“不变”).
(4)四种金属活泼性由强到弱的顺序是D>A>B>C.
(5)A、C形成合金,露置在潮湿空气中,A先被腐蚀.
5.下列叙述正确的是( )
| A. | 聚乙烯能使溴水褪色 | |
| B. | 葡萄糖能发生氧化反应和水解反应 | |
| C. | CH2═CHCN通过缩聚反应得到腈纶 | |
| D. | 区别棉花和羊毛的最简单方法是灼烧闻气味 |
15.下列反应的离子方程式书写不正确的是( )
| A. | 镁条与稀盐酸反应:Mg+2H+═H2↑+Mg 2+ | |
| B. | 铝丝与硫酸铜溶液反应:Al+Cu 2+═Al 3++Cu | |
| C. | 铜丝与硝酸银溶液反应:Cu+2Ag+═2Ag+Cu 2+ | |
| D. | 锌和氯化铜溶液反应:Zn+Cu2+═Zn 2++Cu |
2.下列转变需加入还原剂的是( )
| A. | Fe2+→Fe3+ | B. | Cl-→Cl2 | C. | Mg(OH)2→MgO | D. | MnO4-→MnO2 |
17.下列物质属于电解质的是( )
| A. | 氯化钠溶液 | B. | 氨水 | C. | 硝酸钾 | D. | 铝制导线 |
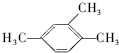 1,3,4-三甲苯
1,3,4-三甲苯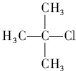 2-甲基-2-氯丙烷
2-甲基-2-氯丙烷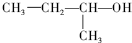 2-甲基-1-丙醇
2-甲基-1-丙醇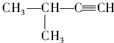 3-甲基-1-丁炔
3-甲基-1-丁炔