题目内容
18.由A、B、C、D四种金属按表中装置图进行实验.| 装置 | 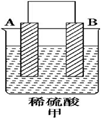 |  | 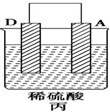 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)装置丙中溶液的pH变大(填“变大”“变小”或“不变”).
(4)四种金属活泼性由强到弱的顺序是D>A>B>C.
(5)A、C形成合金,露置在潮湿空气中,A先被腐蚀.
分析 (1)甲中二价金属A不断溶解,则A为负极,失去电子;
(2)乙中C的质量增加,则B为负极,C为正极,C上铜离子得到电子;
(3)丙中A上有气体产生,则D为负极,A为正极,正极上氢离子得到电子;
(4)一般原电池中负极金属活泼,以此比较金属性;
(5)A、C形成合金,露置在潮湿空气中,发生电化学腐蚀,活泼金属失去电子先被腐蚀.
解答 解:(1)甲中二价金属A不断溶解,则A为负极,失去电子,则负极的电极反应式是A-2e-═A2+,故答案为:A-2e-═A2+;
(2)乙中C的质量增加,则B为负极,C为正极,C上铜离子得到电子,正极的电极反应式为Cu2++2e-═Cu,故答案为:Cu2++2e-═Cu;
(3)丙中A上有气体产生,则D为负极,A为正极,正极上氢离子得到电子,氢离子浓度减小,则pH变大,故答案为:变大;
(4)一般原电池中负极金属活泼,由甲可知金属性为A>B,乙中为B>C,丙中为D>A,则金属性为D>A>B>C,故答案为:D>A>B>C;
(5)A、C形成合金,露置在潮湿空气中,发生电化学腐蚀,活泼金属失去电子先被腐蚀,由金属性D>A>B>C,可知A作负极先被腐蚀,故答案为:A.
点评 本题考查原电池的原理及应用,为高频考点,把握原电池中正、负极的判断、电极反应等为解答的关键,侧重分析和应用能力的考查,注意金属性比较方法,题目难度不大.

练习册系列答案
相关题目
8.下列关于混合物、强电解质、弱电解质和非电解质的组合正确的是( )
| 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 氨水 | H2SO4 | CH3COOH | 干冰 |
| B | 盐酸 | 氢氧化钠 | H2SO4 | SO2 |
| C | 纯碱 | BaSO4 | H2S | 空气 |
| D | 氢氧化钠溶液 | 石灰石 | 熔融NaCl | 氯气 |
| A. | A | B. | B | C. | C | D. | D |
13.某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )


| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 | |
| D. | a和b用导线连接时,电子由铜片通过导线流向铁片 |
3.有8种物质:①甲烷;②苯;③聚乙烯;④2-丁炔;⑤乙醇;⑥邻二甲苯;⑦环己烯;⑧乙醛.既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ③④⑤⑧ | B. | ④⑤⑧ | C. | ③④⑤⑦⑧ | D. | ④⑦⑧ |
10.燃料电池是一种新型电池,能够把化学能转化为电能.某甲烷氧气燃料电池的基本反应是X极:O2(g)+2H2O+4e-═4OH-;Y极:CH4(g)-8e-+10OH-═CO${\;}_{3}^{2-}$+7H2O.下列判断中正确的是( )
| A. | Y极是正极 | B. | X极发生氧化反应 | ||
| C. | 电子由X极经外电路流向Y极 | D. | 此电池的电解质溶液呈碱性 |
5.下列离子方程式正确的是( )
| A. | 向醋酸中滴加氢氧化钠:H++OH-=H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | Ca(HCO3)2溶液与少量KOH溶液反应Ca2++HCO3-+OH-=H20+CaCO3↓ | |
| D. | 向Na2SO3溶液中通入少量氯气:SO32-+Cl2+H2O=SO42-+2Cl-+2H+ |

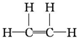 ,F是
,F是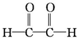 .
. +H2O.
+H2O.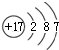 ②CCl4的结构式:
②CCl4的结构式: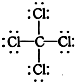
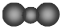 ④Na2S的电子式:
④Na2S的电子式:
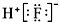 ⑦I-131:7853I
⑦I-131:7853I ⑨乙烯的结构简式:CH2CH2.
⑨乙烯的结构简式:CH2CH2.