题目内容
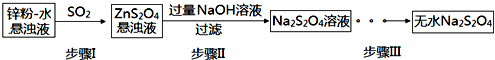
14.以下是某学习小组对乙二酸的某些性质进行研究性学习的过程:[研究课题]探究乙二酸的某些性质
[查阅资料]乙二酸(HOOC-COOH)俗称草酸,草酸晶体的化学式为H2C2O4•2H2O;草酸在100℃时开始升华,157℃时大量升华,并开始分解;草酸蒸气在低温下可冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清石灰水变浑浊.
[提出猜想]
猜想一:乙二酸具有不稳定性
根据草酸晶体的组成,该小组同学猜想其受热分解产物为CO、CO2和H2O. 设计方案:
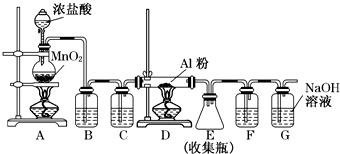
(1)请用下列装置组成一套探究 并验证其产物的实验装置(草酸晶体分解装置略,连接导管略去)
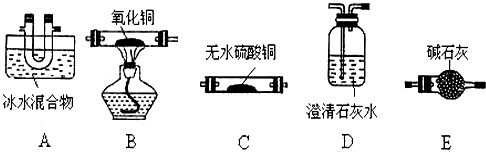
请回答下列问题:
①装置的连接顺序为:A→C→D→E→B→D
②实验时,在点燃B处酒精灯之前,应进行的操作是收集D处气体,检验CO气体的纯度.装置中碱石灰的作用是除去气体中的CO2和水,提高CO的浓度. 检验产物中有CO的实验现象 是B中黑色固体变红色,D中澄清石灰水变浑浊.
③整套装置存在不合理之处为没有一氧化碳尾气处理装置.
猜想二:乙二酸具有还原性设计方案:
(2)该小组同学向酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色并
产生一种气体,从而判断草酸具有较强的还原性.该反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
分析 (1)①猜想其产物为CO、CO2和H2O,草酸在100℃时开始升华,157℃时大量升华,并开始分解.草酸钙不溶于水、草酸蒸气能使澄清石灰水变浑浊、草酸蒸气在低温下可冷凝为固体,分析可知先冷凝挥发出的草酸,再检验水蒸气的生成,检验二氧化碳的生成,并除去二氧化碳,再通过灼热的氧化铜检验一氧化碳气体的存在,利用反应后生成的二氧化碳通入澄清石灰水变浑浊证明一氧化碳的存在;
②CO为可燃性气体,加热之前必须验纯,碱石灰可以吸收草酸分解产生的二氧化碳和水,进而提高CO的浓度,检验产物中CO的实验现象是B中黑色氧化铜变红色,生成了澄清石灰水变浑浊的气体;
③一氧化碳有毒,会污染空气,需要吸收处理装置;
(2)依据氧化还原反应元素化合价变化和电子守恒、原子守恒配平得到反应的离子方程式.
解答 解:(1)①分解产物为CO、CO2和H2O,检验时应该先用无水硫酸铜检验水蒸气,然后用澄清石灰水检验二氧化碳,最后用加热的CuO和澄清石灰水检验CO,所以仪器的连接顺序为:A→C→D→E→B→D,
故答案为:C;E;
②CO为可燃性气体,加热之前必须验纯,所以在点燃B处酒精灯之前必须验纯,碱石灰可以吸收草酸分解产生的二氧化碳和水,进而提高CO的浓度,当装置B中黑色固体变成红色,且装置D澄清石灰水变浑浊,则证明混合气体中含有CO,
故答案为:收集D处气体,检验CO气体的纯度;除去气体中的CO2 和水,提高CO的浓度;B中黑色固体变红色,D中澄清石灰水变浑浊;
③一氧化碳有毒污染空气,需要吸收处理装置,一氧化碳尾气的处理方法为点燃,操作时将气体通到酒精灯火焰上燃烧,
故答案为:没有一氧化碳尾气处理装置;
(2)根据氧化还原反应方程式的配平原则:锰元素化合价+7价变化为+2价,电子转移5,草酸中碳元素化合价+3价变化为+4价,得失电子守恒、质量守恒和电荷守恒配平该反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
点评 本题考查了性质实验方案设计的方法,涉及化学实验、氧化还原反应、离子反应等知识,题目难度中等,注意掌握探究物质性质实验方案设计的方法,明确物质性质及实验操作方法为解答关键,试题有利于提高学生的分析、理解能力及化学实验能力.

| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ⅠFe(s)+CO2(g)=FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ⅡFe(s)+H2O(g)=FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ⅢCO(g)+H2O(g)=CO2(g)+H2(g) | K3 | ? | ? |
(1)反应Ⅰ是吸热(选填“吸热”,“放热”)反应.根据反应Ⅰ与Ⅱ可以推导出同温下K1、K2与K3之间的关系,则K3=$\frac{{K}_{2}}{{K}_{1}}$(用K1、K2表示).
(2)973K时,若反应Ⅲ在一个容积为2L的反应容器内2min时达到平衡,有3mol电子发生转移,则在2min内v(CO2)=0.375mol•(L•s)-1.若压缩容器的容积为原来的一半,平衡将不移动(选填“向左”,“向右”,“不”),CO2的浓度将增大(选填“增大”,“减小”,“不变”).使该反应的平衡转化率及平衡常数都增大的措施有降低温度.
| A. | 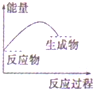 | B. | 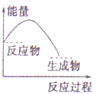 | C. | 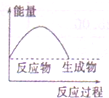 | D. | 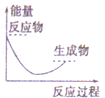 |
 2C,在反应过程中C的物质的量分数随温度变化如图所示:
2C,在反应过程中C的物质的量分数随温度变化如图所示: