题目内容
同温同压下,相同质量的下列气体中体积最大的是( )
| A、N2 |
| B、O2 |
| C、Cl2 |
| D、CO2 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:同温同压下,气体摩尔体积相等,气体体积V=nVm=
Vm,据此分析解答.
| m |
| M |
解答:
解:同温同压下,气体摩尔体积相等,气体体积V=nVm=
Vm,根据
Vm知,相同条件下、相同质量的不同气体,其体积与摩尔质量成反比,如果气体体积最大,则气体摩尔质量应该最小,氮气、氧气、氯气、二氧化碳摩尔质量分别是28g/mol、32g/mol、71g/mol、44g/mol,摩尔质量最小的是氮气,则气体体积最大的是氮气,
故选A.
| m |
| M |
| m |
| M |
故选A.
点评:本题考查阿伏伽德罗定律及其推论,明确物质的量公式中各个物理量的关系是解本题关键,注意气体摩尔体积适用范围及适用条件,为易错点.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列过程不需要通电就能进行的是( )
| A、电化学腐蚀 | B、电镀 |
| C、电解 | D、电泳 |
五种短周期元素的部分性质数据如下:下列叙述正确的是( )
| 元素 | T | X | Y | Z | W |
| 原子半径/nm | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
| A、X的阴离子半径小于T的阳离子半径 |
| B、Y的氢化物的热稳定性比Z的氢化物的大 |
| C、Y单质与Fe反应生成的化合物中,铁元素显+3价 |
| D、Z元素的氧化物对应的水化物一定为强酸 |
有关物质的性质可以用元素周期律解释的是( )
| A、酸性:HCl>H2S>H2O |
| B、密度:Na>K>Li |
| C、沸点:NH3>AsH3>PH3 |
| D、稳定性:HF>HCl>HBr |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol苯分子含有3NA个C-C键 |
| B、一定条件下,1mol N2和3mol H2充分混合,反应后转移的电子数为6NA |
| C、常温下,78.0g Na2O2与58.5g NaCl所含阴离子数相等 |
| D、标准状况下,2.24L CCl4所含分子数为0.1 NA |
下列离子方程式中正确的是( )
| A、盐酸中加入碳酸钙:CO32-+2H+=H2O+CO2↑ |
| B、在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液:NH4++OH-=NH3?H2O |
| C、用氨水吸收过量的二氧化硫:NH3?H2O+SO2=NH4++HSO3- |
| D、氯化亚铁溶液中加入硝酸:2Fe2++4H++NO3-=2Fe3++2H2O+NO↑ |
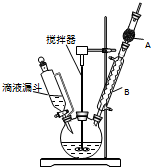 三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.
三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.