题目内容
下列推断合理的是( )
| A、氯化铝和氯化铁在水中都能形成胶体,都可用作净水剂 |
| B、金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| C、浓HNO3有强氧化性,常温下能与Fe发生剧烈反应 |
| D、将SO2通入溴水,溴水褪色后加热能恢复原色 |
考点:硝酸的化学性质,胶体的重要性质,二氧化硫的化学性质
专题:
分析:A.胶体能吸附水中的悬浮物而净水;
B.组成金刚石的元素是C,金刚石燃烧生成二氧化碳;
C.浓硝酸具有强氧化性,常温下能和铁、Al发生钝化现象;
D.二氧化硫具有还原性,能被溴氧化生成硫酸.
B.组成金刚石的元素是C,金刚石燃烧生成二氧化碳;
C.浓硝酸具有强氧化性,常温下能和铁、Al发生钝化现象;
D.二氧化硫具有还原性,能被溴氧化生成硫酸.
解答:
解:A.氯化铁、氯化铝都是强酸弱碱盐,Fe3+、Al3+都能水解生成氢氧化物胶体,胶体具有吸附性,能吸附水中的悬浮物而净水,所以氯化铁、氯化铝可以作净水剂,故A正确;
B.组成金刚石的元素是C,在一定条件下金刚石燃烧生成二氧化碳,故B错误;
C.浓硝酸具有强氧化性,常温下能和铁、Al反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,故C错误;
D.二氧化硫具有还原性,能被溴氧化生成硫酸,SO2+Br2+2H2O=2HBr+H2SO4,所以将SO2通入溴水,溴水褪色后加热不能恢复原色,故D错误;
故选A.
B.组成金刚石的元素是C,在一定条件下金刚石燃烧生成二氧化碳,故B错误;
C.浓硝酸具有强氧化性,常温下能和铁、Al反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,故C错误;
D.二氧化硫具有还原性,能被溴氧化生成硫酸,SO2+Br2+2H2O=2HBr+H2SO4,所以将SO2通入溴水,溴水褪色后加热不能恢复原色,故D错误;
故选A.
点评:本题考查硝酸、二氧化硫、氯化铁、金刚石的反应,明确物质的性质是解本题关键,注意二氧化硫漂白性和还原性的区别,知道钝化现象不是不反应,为易错点.

练习册系列答案
相关题目
有机物分子中原子间(或原子与原子团间)的相互影响对物质性质的改变有时是很显著的.下列各项的事实不能说明上述观点的是( )
| A、甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色 |
| B、乙烯能发生加成反应,而乙烷不能发生加成反应 |
| C、苯酚与浓溴水直接就可反应,而苯与液溴反应还需要加铁屑作催化剂 |
| D、苯酚能与氢氧化钠反应,而乙醇不能与氢氧化钠反应 |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、原子半径:A>B>D>C |
| B、原子序数:d>c>b>a |
| C、离子半径:C3->D->B+>A2+ |
| D、原子的最外层电子数目:A>B>D>C |
将钠块放在坩埚中加热,可观察到的实验现象为( )
①钠块熔化 ②在空气中燃烧产生黄色火焰 ③生成白色固体④生成淡黄色固体 ⑤燃烧时放出大量白烟.
①钠块熔化 ②在空气中燃烧产生黄色火焰 ③生成白色固体④生成淡黄色固体 ⑤燃烧时放出大量白烟.
| A、①②③ | B、①②④ |
| C、②④⑤ | D、①③⑤ |
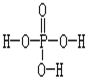 磷酸的结构式如图所示,磷酸分子与磷酸分子的羟基之间可以脱去水.三个磷酸分子可以脱去两个水分子生成三聚磷酸.含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )
磷酸的结构式如图所示,磷酸分子与磷酸分子的羟基之间可以脱去水.三个磷酸分子可以脱去两个水分子生成三聚磷酸.含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )| A、Na5P3O1212mol |
| B、Na3H2P3O10 9mol |
| C、Na5P3O109mol |
| D、Na2H3P3O10 12mol |
赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu2O+Cu2S
6Cu+SO2↑.对于该反应,下列说法正确的是( )
| ||
| A、该反应的氧化剂只有Cu2O |
| B、还原产物与氧化产物的物质的量之比为1:6 |
| C、Cu2S在反应中既是氧化剂,又是还原剂 |
| D、Cu既是氧化产物又是还原产物 |