题目内容
11.化学与生产、生活、社会密切相关.下列说法正确的是( )| A. | SO2具有还原性,可用于蔗糖脱色 | |
| B. | 双氧水具有强氧化性,可用于杀菌消毒 | |
| C. | 铁粉表面积大,可用作食品干燥剂 | |
| D. | SiO2具有导电性,可用于制造光导纤维 |
分析 A.二氧化硫有毒;
B.强氧化性物质能使蛋白质变性;
C.铁与氧气、水反应;
D.二氧化硅为绝缘体.
解答 解:A.二氧化硫有毒,不能用于食品脱色,故A错误;
B.双氧水具有强氧化性,可用于杀菌消毒,故B正确;
C.用铁粉作食品干燥剂是铁与氧气、水共同作用,与表面积大无关,故C错误;
D.二氧化硅为绝缘体,不导电,故D错误;
故选:B.
点评 本题考查了生活中常见的化学知识,明确二氧化硫、过氧化氢、二氧化碳、铁的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
1.下列实验装置,其中按要求设计正确的是( )
| A. |  电解饱和食盐水 | B. | 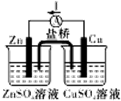 铜锌原电池 | ||
| C. | 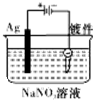 电镀银 | D. | 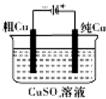 电解精炼铜 |
19.如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中.下列分析正确的是( )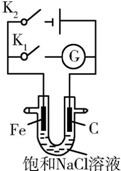

| A. | K1闭合,铁棒上发生的反应为2H++2e-═H2↑ | |
| B. | K1闭合,石墨棒周围溶液的pH逐渐降低 | |
| C. | K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 | |
| D. | K2闭合,电路中通过0.002NA个电子时,两极共产生0.002 mol气体 |
6.下列有关钠的叙述正确的是( )
| A. | 金属钠着火时,不能用水来扑灭,可用CO2灭火 | |
| B. | 钠跟CuSO4溶液反应生成的蓝色沉淀上有时会出现暗斑,这是因为析出了金属铜 | |
| C. | 钠在化学反应中常常失去电子被氧化,作氧化剂,故Na+具有强氧化性 | |
| D. | 2.3 g钠与97.7 g水反应后溶液中溶质的质量分数大于4% |
16.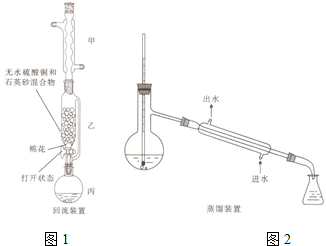 苯甲酸(
苯甲酸(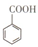 )和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:
)和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:
实验方案为:
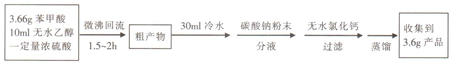
(1)仪器甲的名称为球形冷凝管.
(2)①往丙中加入药品的顺序为C.
A.无水乙醇、浓硫酸、苯甲酸晶体 B.浓硫酸、苯甲酸晶体、无水乙醇
C.苯甲酸晶体、无水乙醇、浓硫酸 D.苯甲酸晶体、浓硫酸、无水乙醇
②若加热反应后发现未加沸石,应采取的正确操作是停止加热,冷却后再加入沸石.
③微沸回流过程中,可以看到乙内的混合试剂的颜色变为蓝色.
(3)加入碳酸钠粉末的作用是中和浓硫酸及未反应的苯甲酸.
(4)分液要用到的玻璃仪器有分液漏斗、烧杯,粗产物在下层(填“上”或“下”).
(5)加热蒸馏若采用2图装置(加热装置已经略去)进行,该装置存在的2个问题为温度计的水银球不应插入反应液中、不应用直型冷凝管.
(6)本实验所得到的苯甲酸乙酯产率为80%.
(7)装置乙的作用为乙中的吸水剂可以吸收反应中产生的水分,有利于提高酯的产率.
 苯甲酸(
苯甲酸( )和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:
)和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解度 | |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶 |
| 乙醇 | 46 | 0.789 | 78.3 | 易溶 |
| 苯甲酸乙酯 | 150 | 1.05 | 212.6 | 难溶 |

(1)仪器甲的名称为球形冷凝管.
(2)①往丙中加入药品的顺序为C.
A.无水乙醇、浓硫酸、苯甲酸晶体 B.浓硫酸、苯甲酸晶体、无水乙醇
C.苯甲酸晶体、无水乙醇、浓硫酸 D.苯甲酸晶体、浓硫酸、无水乙醇
②若加热反应后发现未加沸石,应采取的正确操作是停止加热,冷却后再加入沸石.
③微沸回流过程中,可以看到乙内的混合试剂的颜色变为蓝色.
(3)加入碳酸钠粉末的作用是中和浓硫酸及未反应的苯甲酸.
(4)分液要用到的玻璃仪器有分液漏斗、烧杯,粗产物在下层(填“上”或“下”).
(5)加热蒸馏若采用2图装置(加热装置已经略去)进行,该装置存在的2个问题为温度计的水银球不应插入反应液中、不应用直型冷凝管.
(6)本实验所得到的苯甲酸乙酯产率为80%.
(7)装置乙的作用为乙中的吸水剂可以吸收反应中产生的水分,有利于提高酯的产率.
3.下列说法正确的是( )
| A. | 金属在反应中只能作还原剂,非金属在反应中只能作氧化剂 | |
| B. | 氧化剂在反应中失去电子,还原剂在反应中得到电子 | |
| C. | 金属离子在反应中可能被氧化、也可能被还原 | |
| D. | 阳离子只有氧化性,阴离子只有还原性 |
20.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,22.4 L H2O含有的分子数为 NA | |
| B. | 28g N2和N4组成的混合气体中含有的原子数为2 NA | |
| C. | 1 mol•L-1A1Cl3溶液中含有的Cl-数目为3 NA | |
| D. | 2.3 g Na与足量水反应,转移的电子数目为0.2 NA |
1.下列关于化学素养的说法中,正确的是( )
| A. | 海水中含有丰富的碘元素,故碘被称为“海洋元素” | |
| B. | 溴化银是一种重要的感光材料,也可用于人工降雨 | |
| C. | 钠在盛有氯气的集气瓶中燃烧,火焰呈苍白色,产物为NaCl;铁在盛有氯气的集气瓶中燃烧,火焰呈棕黄色,产物为FeCl3 | |
| D. | 工业炼铁的设备是炼铁高炉,过程中加入石灰石的作用是除脉石(SiO2)造渣 |