题目内容
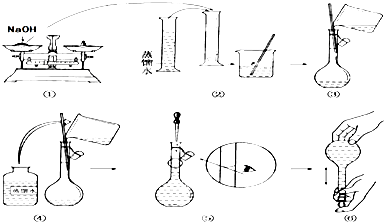
除去镁粉中混有的少量铝粉,可选用的试剂是( )
| A、稀盐酸 | B、稀硫酸 |
| C、氢氧化钠溶液 | D、氨水 |
考点:物质的分离、提纯的基本方法选择与应用
专题:
分析:铝粉可与NaOH溶液反应生成可溶于水的偏铝酸钠,而镁与NaOH溶液不反应,则混合物可用NaOH溶液除杂.
解答:
解:A.盐酸和镁、铝都反应,不能用于除杂,故A错误;
B.硫酸和镁、铝都反应,不能用于除杂,故B错误;
C.铝粉可与NaOH溶液反应生成可溶于水的偏铝酸钠,而镁与NaOH溶液不反应,反应后过滤可除杂,故C正确;
D.镁粉、铝粉与氨水都不反应,不能用于除杂,故D错误.
故选C.
B.硫酸和镁、铝都反应,不能用于除杂,故B错误;
C.铝粉可与NaOH溶液反应生成可溶于水的偏铝酸钠,而镁与NaOH溶液不反应,反应后过滤可除杂,故C正确;
D.镁粉、铝粉与氨水都不反应,不能用于除杂,故D错误.
故选C.
点评:本题考查Mg、Al的化学性质及物质的除杂,把握物质性质的差异及除杂原则为解答的关键,注意发生的化学反应及Al与强碱溶液反应,题目难度不大.

练习册系列答案
相关题目
某小组为研究原电池原理,设计如图Ⅰ、Ⅱ装置,下列叙述正确的是( )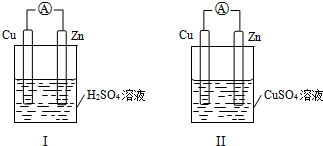

| A、装置Ⅰ,铜片上有O2逸出 |
| B、装置Ⅰ,锌片溶解,发生还原反应 |
| C、装置Ⅱ,电池反应为:Zn+Cu2+=Zn2++Cu |
| D、装置Ⅱ,外电路中,电子从铜电极流向锌电极 |
有机物R结构如图所示,下列说法正确的是( )


| A、R在碱性条件下的水解产物难溶于水 |
| B、R分子中有7种化学环境均不同的氢原子 |
| C、R和溴水反应后所得产物的化学式为C11H12O3Br2 |
| D、R不能使酸性高锰酸钾溶液褪色 |
下列有关溶液组成的描述合理的是( )
| A、无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- |
| B、0.1mol?L-1FeCl3溶液中大量存在Fe2+、NH4+、SCN-、SO42- |
| C、0.1mol?L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- |
| D、中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- |
菜谱中记载:河虾不宜与西红柿同食.主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷.下列说法中正确的是( )
| A、在该反应中维生素C作催化剂 |
| B、砒霜是砷的氧化物,由上述信息可推知砒霜中含有的砷可能是+3价砷 |
| C、因为河虾中含有砷元素,所以不能食用 |
| D、上述反应中维生素C作氧化剂 |