题目内容
7.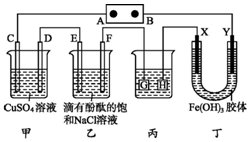 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答:
(1)A极是电源的正极,一段时间后,甲中溶液的PH减小(填增大 减小或不变),丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明Fe(OH)3胶粒在电场作用下向Y极移动.
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为1:2:2:2.
(3)现用丙装置给铜件镀银,则H应是镀件,电镀液是AgNO3溶液.
分析 (1)将直流电源接通后,F极附近呈红色,说明F电极为阴极,阴极上氢离子放电导致F电极附近呈碱性,则C、E、G为阳极,D、F、H为阴极,阴极连接原电池负极,甲中阳极上OH-放电,阴极上Cu2+放电,胶体具有电泳现象,据此回答;
(2)根据转移电子相等进行计算其物质的量之比;
(3)电镀时,镀层Ag为阳极、镀件Cu为阴极,电解质溶液为AgNO3溶液,根据转移电子相等计算析出Ag的质量.
解答 解:(1)将直流电源接通后,F极附近呈红色,说明F电极为阴极,阴极上氢离子放电导致F电极附近呈碱性,则C、E、G为阳极,D、F、H为阴极,阴极连接原电池负极,所以B是原电池负极,A极是电源的正极;甲中阳极上OH-放电,甲中溶液的pH减小,丁中阳极X极附近的颜色逐渐变浅,阴极Y极附近的颜色逐渐变深,这表明 Fe(OH)3胶粒在电场作用下向Y极移动,
故答案为:正极;减小;Fe(OH)3胶粒;
(2)C、D、E、F发生的反应分别为:4OH--4e-=2H2O+O2↑、Cu2++2e-=Cu、2Cl--2e-=Cl2↑、2H++2e-=H2↑,串联电路中转移电子相等,假设都转移4mol电子时,O2、Cu、Cl2、H2的物质的量分别是1mol、2mol、2mol、2mol,所以生成单质的物质的量之比为1:2:2:2,故答案为:1:2:2:2;
(3)用丙装置给铜件镀银,镀层Ag为阳极,则G为Ag,镀件H为阴极,阴极材料是Cu,电镀液为AgNO3溶液,故答案为:镀件;AgNO3.
点评 本题考查了电解池原理,明确离子放电顺序是解本题关键,根据各个电极上发生的反应来分析解答,难点是电极反应式的书写,题目难度中等.

练习册系列答案
相关题目
2.设NA表示阿伏加德罗常数,下列说法中错误的是( )
| A. | 142g氯气中含Cl2的分子数为2NA | |
| B. | 1.7gOH-中所含电子的数目为NA | |
| C. | 49g硫酸中所含氧原子的数目为2NA | |
| D. | 71g硫酸钠中所含钠离子的数目为2NA |
19.化学与生活、生产、环境等密切相关.下列叙述不正确的是( )
| A. | 可用聚氯乙烯代替乙烯制作食品包装袋 | |
| B. | 去除银器表面Ag2S,可将银器放在盛有食醋的铝锅中煮沸片刻 | |
| C. | 开发核能、太阳能等新能源,推广甲醇汽油,使用无磷洗涤剂都符合环保理念 | |
| D. | “连续纤维增韧”航空材料主要是由碳化硅、陶瓷和碳纤维复合而成,是一种新型无机非金属材料 |

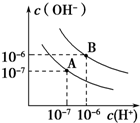 已知水在25℃和95℃时,其电离平衡曲线如图所示:
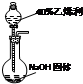
已知水在25℃和95℃时,其电离平衡曲线如图所示: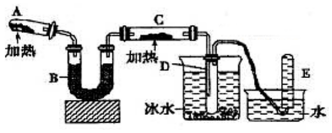 己知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应.
己知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应.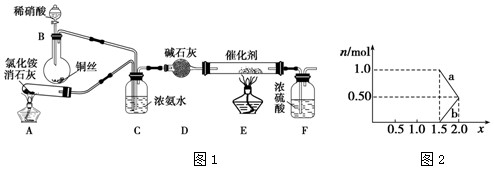

 )
) .
. .
.