题目内容
10.有关化学与生产、生活相关的叙述正确的是( )| A. | 碘酒能消毒是利用碘的还原性 | |
| B. | 葡萄糖注射液不能产生丁达尔效应,不属于胶体 | |
| C. | 14C可用于文物的年代鉴定,14C与12C互为同素异形体 | |
| D. | 某溶液中加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32- |
分析 A.碘单质有氧化性;
B.丁达尔效应是胶体特有的性质;
C.同素异形体研究对象为单质;
D.碳酸氢根、亚硫酸根离子等都能与盐酸反应生成能使澄清石灰水变浑浊的气体.
解答 解:A.碘单质有氧化性,能杀菌消毒,故A错误;
B.葡萄糖注射液为溶液,不能产生丁达尔效应,不属于胶体,故B正确;
C.14C与12C互为同位素,故C错误;
D.某溶液中加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中不一定含有CO32-,还可能为碳酸氢根离子、亚硫酸根离子等,故D错误;
故选:B.
点评 本题考查了化学知识在生活中的应用,熟悉相关物质的性质是解题关键,难度不大,属于识记型知识,注意归纳总结.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
20.下列实验现象与氧化还原反应有关的是( )
| A. | 将NO2通入水中,气体由红棕色逐渐转变为无色 | |
| B. | 向澄清的石灰水中通入SO2,有白色沉淀形成 | |
| C. | NH3使湿润的红色石蕊试纸变蓝 | |
| D. | 向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
1.下列说法正确的是( )
| A. | 含碳元素的化合物都是有机物 | |
| B. | 苯的同系物能使KMnO4酸性溶液褪色 | |
| C. | 石油分馏可获得乙烯、丙烯和丁二烯 | |
| D. | 酯类和醇类均能发生水解反应 |
18.如图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑.下列说法错误的是( )
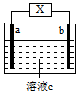

| A. | a、b不可能是同种材料的电极 | |
| B. | X为电流计,c为稀盐酸,该装置为原电池 | |
| C. | X为直流电源,c为稀硫酸,该装置为电解池 | |
| D. | X为电流计,c为稀硫酸,a可能为铜电极,b可能为锌电极 |
5.下列有关说法不正确的是( )
| A. | 分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液 | |
| B. | 将纳米材料(微粒直径是1nm-100nm)分散到分散剂中得到的分散系有丁达尔效应 | |
| C. | 氢氧化铁胶体的制备方法是:将氢氧化铁固体溶于沸水中继续煮沸 | |
| D. | 浊液与其它分散系的本质区别是浊液的分散质粒子的直径大于100nm |
15.在某温度时,测得纯水中的c(H+)=5.0×10-7 mol•L-1,则c(OH-)为( )
| A. | 5.0×10-7 mol•L-1 | B. | 1.0×10-7 mol•L-1 | ||
| C. | 1.0×10-14/5.0×10-7 mol•L-1 | D. | 无法确定 |
2.下列事实不能用勒夏特列原理解释的是( )
| A. | 溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 | |
| B. | 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 | |
| C. | 反应CO(g)+NO2 (g)?CO2 (g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 | |
| D. | 对于2HI(g)?H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.lmol Fe在0.lmolCl2中充分燃烧,转移的电子数为0.3NA | |
| B. | 25℃时,pH=13的1.0 LBa(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 含NA个氧原子的O2与含NA个氧原子的O3的质量比为2:3 | |
| D. | lmol CnH2n+2分子中含共价键数目为(3n+1)NA |