题目内容
10.若配制0.5mol•L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,下列所配制的硫酸溶液浓度偏低的是 ( )| A. | 将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒. | |
| B. | 稀释后没冷却到室温就将溶液转移至容量瓶. | |
| C. | 用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切. | |
| D. | 用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切 | |
| E. | 移液时容量瓶中有少量蒸馏水 |
分析 依据c=$\frac{n}{V}$分析,凡是能够使溶质的物质的量n偏小或者溶液的体积V偏大的操作,都会使溶液的浓度偏低,反之,溶液的浓度偏高,据此分析解答.
解答 解:A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,导致配制的溶液中溶质的物质的量偏小,根据c=$\frac{n}{V}$可得,配制的溶液浓度偏低,故A正确;
B.稀释后没冷却到室温就将溶液转移至容量瓶,热的溶液体积偏大,冷却后溶液的体积变小,则配制的溶液体积偏小,根据cc=$\frac{n}{V}$可得,配制的溶液浓度偏高,故B错误;
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,导致配制的溶液体积偏大,根据c=$\frac{n}{V}$可得,配制的溶液浓度偏低,故C正确;
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切,导致加入的蒸馏水体积低于容量瓶刻度线,配制的溶液体积偏小,根据c=$\frac{n}{V}$可得,溶液浓度偏高,故D错误;
E.移液时容量瓶中有少量蒸馏水,对溶质的物质的量及最终溶液的体积都没有影响,所以不影响配制结果,故E错误;
故选AC.
点评 本题考查了配制一定物质的量浓度的溶液过程中的误差分析,为中等难度的试题,试题基础性强,难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,注意明确误差分析的方法.

练习册系列答案
相关题目
20.下列说法正确的是( )
| A. | 某试样焰色反应呈黄色,则该试样一定是钠的化合物 | |
| B. | 在石油蒸馏装置中,将温度计水银球插入液面以下 | |
| C. | 在鸡蛋白溶液中加入浓的Na2SO4溶液,可使蛋白质变性 | |
| D. | 用结晶的方法分离氯化钠和硝酸钾的混合物 |
1.将一小块钠投入下列溶液时,既能产生气体又会出现沉淀的是( )
| A. | 稀H2SO4 | B. | 氢氧化钠溶液 | C. | 氯化铁溶液 | D. | 氯化钾溶液 |
18.下列有关溶液的存储和配制的描述不正确的是( )
| A. | 氨水易挥发,应密封在低温处保存 | |
| B. | 水玻璃可存放在橡胶塞的细口瓶中 | |
| C. | 配制FeCl3溶液,先加浓盐酸溶解氯化铁固体,再稀释至相应浓度 | |
| D. | 称取2.5g硫酸铜晶体,溶于l00mL水中可以配制物质的量浓度为0.1mol•L-1的硫酸铜溶液 |
5.下列说法正确的是( )
| A. | 28g N2含有的原子数为NA | |
| B. | 4gCa变成Ca2+失去的电子数为0.1NA | |
| C. | 1molO2的质量等于1mol O的质量 | |
| D. | 24gO2和24gO3所含有的原子数目相等 |
15.已知:NA表示阿伏加德罗常数,则下列说法不正确的是( )
| A. | 31g白磷分子中所含p-p共价键数目为1.5NA | |
| B. | 标准状况下,2.24LD2中所含中子的数目是0.2NA | |
| C. | 常温常压下42g乙烯和丙烯的混合气体含氢原子数目为6 NA | |
| D. | 常温下,向1L0.2mol/L的盐酸溶液通入氨气,当溶液PH=7时,溶液中NH4+的数目小于0.2NA |
19.下列实验装置设计正确、且能达到目的是( )
| A. | 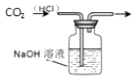 用于除去CO2中的HCl | B. | 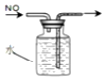 排水法收集NO | ||
| C. | 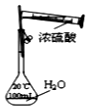 配制一定物质的量浓度的稀硫酸 | D. | 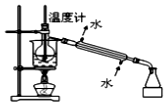 海水的淡化 |
9.某原子的摩尔质量是Mg•mol-1,则一个该原子的真实质量是( )
| A. | $\frac{M}{6.02×1{0}^{23}}$g | B. | $\frac{1}{M}$ g | C. | M g | D. | $\frac{6.02×1{0}^{23}}{M}$ g |