题目内容
已知反应:2HBr(g)  Br2(g)+H2(g),在四种不同的条件下进行,Br2、H2起始的浓度为0,反应物HBr的浓度(mol/L)随反应时间(min)的变化情况如下表:
Br2(g)+H2(g),在四种不同的条件下进行,Br2、H2起始的浓度为0,反应物HBr的浓度(mol/L)随反应时间(min)的变化情况如下表:
|
实验序号 |
实验温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
800℃ |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
3 |
800℃ |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
下列说法正确的是( )
A.从上表数据分析,2HBr(g)
 Br2(g)+H2(g)正反应为放热反应
Br2(g)+H2(g)正反应为放热反应
B.实验2中HBr的初始浓度C2=1.0 mol/L
C.实验3反应速率小于实验1的反应速率
D.实验4一定使用了催化剂
【答案】
B
【解析】
试题分析:根据实验1、4可以判断,升高温度,平衡正向移动,所以正反应是吸热反应,A、D错误;根据实验1、2可以看出温度相同,平衡时HBr浓度相同,说明起始时HBr浓度相同,则C2=1.0 mol/L,B正确;根据实验1、3可以看出温度相同,实验3平衡时HBr的浓度比实验1大,说明起始时实验3的HBr浓度大于实验1的HBr浓度,所以实验3的速率大于实验1的速率,C错误。答案选B。
考点:化学平衡移动
点评:本题属于典型的控制变量研究物质的性质题,在高考中很热点。

练习册系列答案
相关题目
已知反应 =2HBr+Se,由此得出的结论错误的是
=2HBr+Se,由此得出的结论错误的是
[ ]
|
A.溴的氧化性比硒强 |
B.HBr比 |
|
C.溴的沸点比硒高 |
D. |
已知反应:2HBr(g)  Br2(g)+H2(g),在四种不同的条件下进行,Br2、H2起始的浓度为0,反应物HBr的浓度(mol/L)随反应时间(min)的变化情况如下表:
Br2(g)+H2(g),在四种不同的条件下进行,Br2、H2起始的浓度为0,反应物HBr的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验序号 | 实验温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
A.从上表数据分析,2HBr(g)
 Br2(g)+H2(g)正反应为放热反应
Br2(g)+H2(g)正反应为放热反应B.实验2中HBr的初始浓度C2=1.0 mol/L
C.实验3反应速率小于实验1的反应速率
D.实验4一定使用了催化剂
 实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷: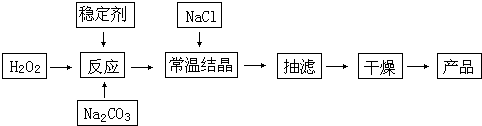
 稳定
稳定 酸性比
酸性比 酸性强
酸性强