题目内容
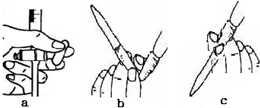
7.氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如图所示的装置.
(1)若分液漏斗中氨水的浓度为9.0mol•L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、量筒、玻璃棒、胶头滴管
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为过氧化钠.
(3)乙装置的作用是干燥氧气和氨气的混合气体;;写出受热时丙装置发生反应的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(4)当戊中观察到紫色石蕊试液变红现象,则说明已制得硝酸.某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因过量的氨气致使戊中溶液不一定呈酸性.如何改进装置在丙和丁之间连接盛有无水氯化钙的干燥管或盛有浓硫酸的洗气瓶.
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是烧瓶内水面慢慢上升,上升到一定高度不再变化,试管内气体颜色由红棕色逐渐变淡至无色;为测定试管丁内硝酸溶液的浓度,从中取10mL溶液于锥形瓶中,用0.1mol•L-1的NaOH溶液滴定.滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是b.
分析 (1)根据配制溶液的操作步骤判断所用仪器;
(2)甲装置不需要加热即能同时产生氨气和氧气,说明固体X溶于氨水即放热又产生氧气;
(3)乙装置为干燥管,作用是干燥氧气和氨气的混合气体;丙装置发生反应的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(4)根据硝酸具有酸性,能使紫色石蕊试液变红判断;没有观察到现象说明溶液不呈酸性,则生成的硝酸与碱发生了反应;在丙和丁之间连接盛有无水氯化钙的干燥管或盛有浓硫酸的洗气瓶除去多余的氨气确保戊溶液呈酸性;
(5)改进后待反应结束,将丁装置收集的为二氧化氮,倒立在盛水的水槽中,二氧化氮与水反应生成一氧化氮和硝酸,据此分析观察到的现象;滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是b.
解答 解:(1)量取浓氨水要用量筒,稀释浓氨水要用烧杯、玻璃棒,配制溶液要用100mL容量瓶,胶头滴管,故答案为:胶头滴管;
(2)甲装置不需要加热即能同时产生氨气和氧气,说明固体X溶于氨水即放热又产生氧气,则该固体为过氧化钠,故答案为:过氧化钠;
(3)乙装置为干燥管,作用是干燥氧气和氨气的混合气体;丙装置发生反应的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:干燥氧气和氨气的混合气体; 4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(4)因为硝酸具有酸性,能使紫色石蕊试液变红,所以当戊中观察到紫色石蕊试液变红,说明已制得硝酸;没有观察到现象说明溶液不呈酸性,则生成的硝酸与过量的氨气发生了反应;在丙和丁之间连接盛有无水氯化钙的干燥管或盛有浓硫酸的洗气瓶除去多余的氨气确保戊溶液呈酸性,
故答案为:紫色石蕊试液变红;过量的氨气致使戊中溶液不一定呈酸性;在丙和丁之间连接盛有无水氯化钙的干燥管或盛有浓硫酸的洗气瓶;
(5)改进后待反应结束,将丁装置收集的为二氧化氮,倒立在盛水的水槽中,二氧化氮与水反应生成一氧化氮和硝酸,所以观察到的现象为烧瓶内水面慢慢上升,上升到一定高度不再变化,试管内气体颜色由红棕色逐渐变淡至无色;滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是b,
故答案为:烧瓶内水面慢慢上升,上升到一定高度不再变化,试管内气体颜色由红棕色逐渐变淡至无色;b.
点评 本题考查了实验室制氨气的原理和装置以及探究硝酸的制备和性质,同时考查了浓硫酸、氨气等物质的性质应用,难度一般.

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案(1)在一密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其化学平衡常数K与温度T的关系如下表:
| T | 298K | 398K | 498K | … |
| K | 4.1×106 | K1 | K2 | … |
②若保持容器的容积不变,则该反应达到化学平衡状态的依据是acd(填序号).
a.2v正(H2)=3v逆(NH3) b.容器内N2、H2和NH3浓度相等的状态
c.容器内压强保持不变 d.混合气体的平均摩尔质量保持不变
③若维持容器的体积不变,达到平衡状态后再向容器中通入一定量的N2,此时逆反应速率不变(填“增大”、“减小”或“不变”);平衡向正反应方向移动(填“正反应”或“逆反应”).
④已知AgCl可溶于氨水中,而AgBr不溶于氨水中,则Ksp(AgCl)> Ksp(AgBr).
(2)肼是氮元素的另一种氢化物,分子式为N2H4.
①写出肼的电子式
 .
.②298K时,1.00g N2H4(l)与足量的N2O4(l)完全反应生成氮气和液态水,放出19.15kJ的热量.写出该反应的热化学方程式2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1225.6kJ/mol.
③肼也可以在纯氧中燃烧生成氮气和水,为了充分利用其能量有人设计了原电池装置,电极材料是多孔石墨电极,电解质为能够传导H+的固体电解质,请写出负极反应式N2H4-4e-═N2+4H+.
| A. | SiO2与CO2相似,由一个硅原子和两个氧原子构成一个SiO2分子 | |
| B. | 硅酸盐一般不溶于水,它是水泥、陶瓷、玻璃的主要成分 | |
| C. | SiO2是酸性氧化物,能和碱反应,不能和酸反应 | |
| D. | 硅元素是构成矿物岩石的主要成分之一,其化合态几乎全部是氧化物和硅酸盐 |

已知:
①20℃时,0.1mol.L-1的金属离子沉淀时的pH
| pH | Fe3+ | Zn2+ | Mn2+ | Cu2+ |
| 开始沉淀 | 1.9 | 6.0 | 8.1 | 4.7 |
| 沉淀完全 | 3.7 | 8.0 | 10.1 | 6.7 |
| 沉淀溶解 | 不溶解 | 10.5 | 不溶解 | / |
③ZnSO4+4NH3═[Zn(NH3)4]SO4,[Zn(NH3)4]SO4易溶于水.
回答下列问题:
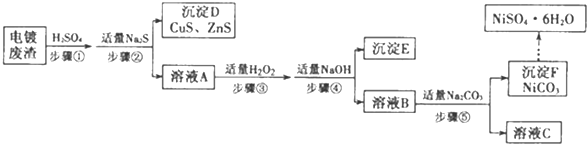
(1)为提高烟尘中金属离子的浸出率,除了适度增加硫酸浓度外,还可以采取什么措施?(举出1种)增大硫酸浓度/升高温度/边加硫酸边搅拦/增加浸出时间等.
(2)上述流程测得溶液pH=5.0,此处可以选择的测量仪器是pH计(或者酸度计或试纸).
(3)加入MnO2的目的是将Fe2+氧化成Fe3+.
(4)写出过二硫酸铵把硫酸锰(MnSO4)氧化的化学方程式MnSO4+(NH4)2S2O8+2H2O=MnO2+(NH4)2SO4+2H2SO4.
(5)写出还原过程发生的主要反应的离子方程式Zn+Cu2+=Zn2++Cu.
(6)操作甲中为使锌离子完全沉淀,添加的最佳试剂是C
A锌粉 B氨水 C( NH4)2CO3 D NaOH
(7)若pH=5.0时,溶液中的Cu2+尚未开始沉淀,求溶液中允许的Cu2+浓度的最大值.
| A. | v(NH3)正=2v(CO2)逆 | B. | 密闭容器中总压强不变 | ||
| C. | 密闭容器中氨气的体积分数不变 | D. | 密闭容器中混合气体的密度不变 |
| A. | 阳极反应为Fe-2e-═Fe2+ | |
| B. | 电路中每转移12mol电子,最多有1molCr2O${\;}_{7}^{2-}$被还原 | |
| C. | 过程中有Fe(OH)3沉淀生成 | |
| D. | 电解过程中溶液pH不会变化 |

常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0 溶解) |
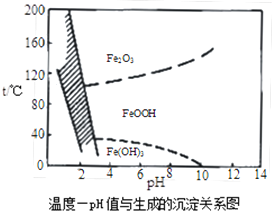
(2)调pH=4.0是为了除去Fe3+
(3)钠离子交换树脂的作用原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+、Al3+、Mg2+
(4)试配平下列氧化还原反应方程式:2Fe2++1H2O2+2H+═2Fe3++2H2O( )
(5)通入SO2的目的是将六价铬元素还原成三价铬元素,生成Cr(OH)(H2O)5SO4.
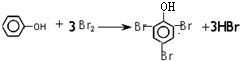 .
. ;
; +
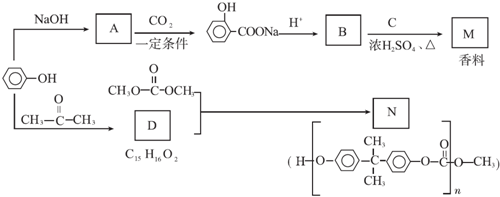
+ $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$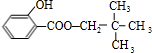 +H2O.
+H2O.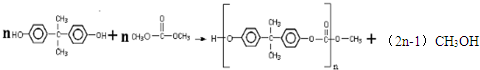 ,反应类型为缩聚反应.
,反应类型为缩聚反应.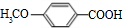 .
.