题目内容
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、2g H2中含有的电子数为2NA |
| B、0.2mol?L-1的FeCl3溶液中,含Fe3+数为0.2NA |
| C、等物质的量的N2和CO所含分子数均为NA |
| D、在密闭容器中加入1molN2和3mol H2,充分反应后可得到NH3分子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氢气分子中含有2个电子,2g氢气的物质的量为1mol,含有2mol电子;
B.没有告诉氯化铁溶液的体积,无法计算溶液中铁离子的数目;
C.没有告诉氮气和一氧化碳的物质的量,无法计算二者含有的电子数;
D.氮气与氢气的反应为可逆反应,反应物不可能完全转化成生成物.
B.没有告诉氯化铁溶液的体积,无法计算溶液中铁离子的数目;
C.没有告诉氮气和一氧化碳的物质的量,无法计算二者含有的电子数;
D.氮气与氢气的反应为可逆反应,反应物不可能完全转化成生成物.
解答:
解:A.2g氢气的物质的量为1mol,1mol氢气含有2mol氢原子,含有2mol电子,含有的电子数为2NA,故A正确;
B.缺少溶液的体积,无法计算溶液中含有的铁离子数目,故B错误;
C.等物质的量,没有告诉具体物质的量数值,无法计算含有的电子数,故C错误;
D.1molN2和3molH2充分反应后生成氨气的物质的量小于2mol,得到NH3分子数小于2NA,故D错误;
故选A.
B.缺少溶液的体积,无法计算溶液中含有的铁离子数目,故B错误;
C.等物质的量,没有告诉具体物质的量数值,无法计算含有的电子数,故C错误;
D.1molN2和3molH2充分反应后生成氨气的物质的量小于2mol,得到NH3分子数小于2NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确分子、原子、原子核内质子中子及核外电子的构成关系,嘻嘻嘻BC为易错点,B中没有告诉溶液体积、C中没有告诉物质的量,试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
根据实验目的判断下列实验操作或装置正确的是( )
A、 精炼铝 |
B、 在铁制品上镀铜 |
C、 配制稀硫酸溶液 |
D、 净化、精制淀粉胶体 |
某无色透明溶液,能与Al作用放出H2,此溶液中可以大量共存的离子组是( )
| A、OH-、Mg2+、Ba2+、Cl- |
| B、SO42-、Na+、HCO3-、K+ |
| C、NO3-、OH-、Cl-、Ba2+ |
| D、Cu2+、H+、SO42-、NO3- |
如图图象分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法正确的是( )
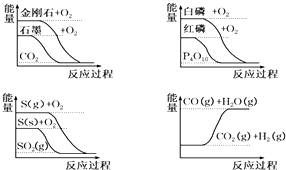

| A、金刚石比石墨稳定 |
| B、白磷转变为红磷是吸热反应 |
| C、相同物质的量的S(g)比S(s)完全反应时放热多 |
| D、CO(g)+H2O(g)═CO2(g)+H2(g) 该反应吸热 |
小明家里收藏了一件清代的铝制佛像,该佛像至今仍保存十分完好.该佛像未被锈蚀的主要原因是( )
| A、铝不易发生化学反应 |
| B、铝的氧化物容易发生还原反应 |
| C、铝被氧化生成的氧化膜稳定且致密,保护着里面的铝 |
| D、铝的氧化物熔点很高 |
下列说法正确的是( )
| A、纤维素、淀粉、蛋白质、油脂在一定条件下都能发生水解反应 |
B、向肉桂醛(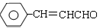 )中滴加酸性高锰酸钾溶液,紫红色很快褪去,此现象可用来证明肉桂醛分子中一定含有醛基 )中滴加酸性高锰酸钾溶液,紫红色很快褪去,此现象可用来证明肉桂醛分子中一定含有醛基 |
| C、亚硫酸氢钠可作为药物用来治疗胃溃疡病人的胃酸过多症 |
| D、铝箔和金箔置于冷的浓硫酸中均无明显现象,两者原理相同 |
在过去,糖尿病的检测方法是把NaOH溶液和CuSO4溶液加入某病人的尿液中,微热时,如果观察到红色沉淀,说明该尿液中含有( )
| A、食醋 | B、白酒 | C、食盐 | D、葡萄糖 |
与CH3CH2OH互为同分异构体的是( )
| A、CH3-O-CH3 |
| B、CH3COOH |
| C、HOCH2CH3 |
| D、CH3CHO |