题目内容
能选用如图装置正确完成的实验是( )


| A、用锌粒与稀硫酸制取并收集H2 |
| B、用生石灰和浓氨水制取并收集NH3 |
| C、用少量MnO2和H2O2制取并收集O2 |
| D、用浓硫酸和浓盐酸制取并收集HCl |
考点:实验装置综合,常见气体制备原理及装置选择
专题:
分析:该装置的反应装置为固液混合不加热型装置,生成的气体可以采用向下排空气法收集,说明生成的气体常温下和空气不反应,且浓度小于空气,据此分析解答.
解答:
解:该装置的反应装置为固液混合不加热型装置,生成的气体可以采用向下排空气法收集,说明生成的气体常温下和空气不反应,且浓度小于空气,
A.锌粒和稀硫酸反应制取氢气的装置属于固液混合不加热型装置,且生成的氢气密度小于空气,常温下和空气不反应,符合条件,故A正确;
B.用生石灰和浓氨水制取氨气的装置属于固液混合不加热型装置,且生成的氨气密度小于空气,常温下和空气不反应,符合条件,故B正确;
C.用少量二氧化锰、双氧水制取氧气的装置属于固液混合不加热型装置,但生成的氧气密度大于空气,不符合条件,故C错误;
D.用浓硫酸和浓盐酸制取HCl的装置属于液液混合不加热型装置,且生成的HCl密度大于空气,不符合条件,故D错误;
故选AB.
A.锌粒和稀硫酸反应制取氢气的装置属于固液混合不加热型装置,且生成的氢气密度小于空气,常温下和空气不反应,符合条件,故A正确;
B.用生石灰和浓氨水制取氨气的装置属于固液混合不加热型装置,且生成的氨气密度小于空气,常温下和空气不反应,符合条件,故B正确;
C.用少量二氧化锰、双氧水制取氧气的装置属于固液混合不加热型装置,但生成的氧气密度大于空气,不符合条件,故C错误;
D.用浓硫酸和浓盐酸制取HCl的装置属于液液混合不加热型装置,且生成的HCl密度大于空气,不符合条件,故D错误;
故选AB.
点评:本题考查气体的制取原理、装置选择等知识点,根据反应特点及气体性质、密度确定反应装置、收集装置,熟练掌握常见气体的制取和收集,题目难度不大.

练习册系列答案
相关题目
设为阿伏加德罗常数的值.下列说法正确的是( )
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | ||
B、标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为
| ||
| C、pH=13的NaOH溶液中含有的OH-为0.1mol | ||
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4 |
下列物质中,主要成分属于硅酸盐的是( )
| A、烧碱 | B、水泥 | C、石灰石 | D、水晶 |
下列反应的离子方程式正确的是( )
| A、澄清的石灰水跟盐酸反应:H++OH-═H2O |
| B、铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
| D、金属钠跟水反应:Na+2H2O═Na++2OH-+H2↑ |
下列关于H2SO3溶液的说法正确的是( )
| A、能使酸性高锰酸钾溶液褪色是因为H2SO3的漂白性 |
| B、H2SO3在空气中容易变质,成为SO2 |
| C、溶液中存在的微粒只有H+和SO32- |
| D、能与NaOH溶液发生复分解反应 |
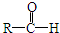 +R′-CH2-CHO→
+R′-CH2-CHO→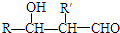 (其中R、R′为烃基,也可以是氢原子)产物不稳定,受热易脱水而生成不饱和醛.
(其中R、R′为烃基,也可以是氢原子)产物不稳定,受热易脱水而生成不饱和醛.