题目内容
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
| A.加成反应 | B.取代反应 | C.水解反应 | D.酯化反应 |
⑷写出制取乙酸乙酯的化学反应方程式:
(8分)(1)防止由于乙醇和乙酸的吸收而造成液体回流(倒吸)(2分,合理答案均给分); (2)BD(选全2分,漏选得1分,多选0分)
(3)吸水剂、催化剂(2分,未答全1分,多答0分)。
(4)CH3COOH+C2H5OH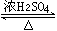 CH3COOC2H5+H2O(2分;未写条件扣1分,未写可逆符号扣1分)
CH3COOC2H5+H2O(2分;未写条件扣1分,未写可逆符号扣1分)
解析试题分析:(1)由于乙醇和乙酸都是易挥发的,所以在乙酸乙酯中含有乙醇和乙酸。又因为二者都是和水互溶的,则装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止由于乙醇和乙酸的吸收而造成液体回流(倒吸)。
(2)乙酸和乙醇生成乙酸乙酯的反应是酯化反应,也是取代反应,答案选BD。
(3)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,因此浓硫酸的作用为催化剂,吸水剂。
(4)该反应的化学方程式是CH3COOH+C2H5OH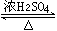 CH3COOC2H5+H2O。
CH3COOC2H5+H2O。
考点:考查乙酸乙酯的制备
点评:该题是基础性试题的考查,难度不大。主要是考查学生对酯化反应原理、实验基本操作的熟悉了解程度,解答时须注意酯化反应的原理和饱和碳酸钠溶液的作用,有利于培养学生的逻辑思维能力和规范的实验设计能力。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案下图是一些常见有机物的转化关系,以下有关反应的说法不正确的是
| A.反应①是加成反应 |
| B.反应②是加聚反应 |
| C.反应③是消去反应 |
| D.反应④⑤⑥是取代反应 |
下列反应中,不属于取代反应的是( )
| A.在催化剂存在条件下苯与溴反应制溴苯 |
| B.苯与浓硝酸、浓硫酸混合共热制取硝基苯 |
| C.乙烯与溴生成1,2二溴乙烷 |
| D.在光照条件下甲烷和氯气反应制氯仿 |
某草药中有一种色素,它的结构简式为 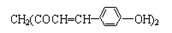 ,用它制成的试剂可以检验物质的酸碱性。能够跟1 mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( ).
,用它制成的试剂可以检验物质的酸碱性。能够跟1 mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( ).
| A.3 mol、5 mol | B.6 mol、8 mol | C.10 mol、8 mol | D.6 mol、10 mol |
糖原[(C6H10O5)n]是一种相对分子质量比淀粉更大的多糖,主要存在于肝脏和肌肉中,常常称为动物淀粉,下列有关糖原的叙述正确的是 ( )。
| A.糖原与纤维素互为同分异构体,与淀粉互为同系物 |
| B.糖原水解的最终产物是葡萄糖 |
| C.糖原具有还原性,是还原性糖 |
| D.肌肉中的肌糖原是肌肉内能量的储备形式,运动需要供能,机体可以直接利用肌糖原 |



