题目内容
11.下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是( )| 选项 | 离子组 | 试剂X | 离子方程式 |
| A | 透明溶液中:Fe3+、NH4+、SO42-、NO3- | 过量的铜粉 | 2Fe3++Cu=2Fe2++Cu2+ |
| B | Fe3+、Al3+、AlO2-、Cl- | 过量的盐酸 | AlO2+4H-=Al3++2H2O |
| C | Na、Ba2+、HCO3-、NO3- | NaHSO4溶液 | H-+HCO3=CO2↑+H2O |
| D | pH=0的溶液中:Mg2+,Fe2+、NO3-、SO42- | 双氧水 | 2Fe2++H2O2+2H-=2Fe3++2H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.该组离子之间不反应,加Cu与铁离子反应;
B.Fe3+、Al3+分别与AlO2-相互促进水解;
C.该组离子之间不反应,加NaHSO4溶液还生成硫酸钡沉淀;
D.pH=0的溶液,显酸性,离子之间发生氧化还原反应.
解答 解:A.透明溶液可能是有色溶液,在透明溶液中这四种离子能大量共存,加入铜粉,铜与铁离子反应,铜不能与亚铁离子反应,发生2Fe3++Cu=2Fe2++Cu2+,故A正确;
B.发生Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓,Al3++3AlO2-+6H2O=4Al(OH)3↓,离子不能大量共存,故B错误;
C.加入硫酸氢钠溶液,相当于加入强酸,漏掉了Ba2++SO42-=BaSO4↓,故C错误;
D.pH=0的溶液为强酸溶液,发生反应为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,离子组不能大量共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
1.下列变化属于化学变化的是( )
①导电性;②瓦斯爆炸;③缓慢氧化;④丁达尔效应;⑤萃取;⑥焰色反应.
①导电性;②瓦斯爆炸;③缓慢氧化;④丁达尔效应;⑤萃取;⑥焰色反应.
| A. | ①②④ | B. | ②③ | C. | ②③⑥ | D. | ②③⑤ |
2.实验室用蓄电池电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极:Pb+SO42-=PbSO4+2e- 正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,今若制得0.05mol Cl2,这时电池内消耗的H2SO4的物质的量至少是( )
| A. | 0.025 mol | B. | 0.050 mol | C. | 0.10 mol | D. | 0.20 mol |
6.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向Na2SiO3溶液中滴加几滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| B | 取久置的Na2O2粉末,向其中滴加过量的盐酸后产生气体 | Na2O2没有变质 |
| C | 溴乙烷与NaOH溶液共热后,加入AgNO3溶液,未出现淡黄色沉淀 | 溴乙烷没有水解 |
| D | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32-强 |
| A. | A | B. | B | C. | C | D. | D |
16.某有机物A在NaOH溶液存在下加热能水解生成B和C,B与盐酸反应生成D,C氧化得E,E继续氧化得D,并测得D能发生银镜反应,则A的名称是( )
| A. | 甲酸甲酯 | B. | 甲酸乙酯 | C. | 乙酸乙酯 | D. | 乙酸甲酯 |
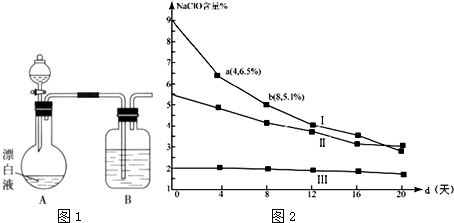
 .
. .
.