题目内容
在恒容的密闭容器中,某一可逆反应A(s)+3B(g)?C(g)+D(g)△H>0在一定温度下达到平衡.则下列说法错误的是( )
| A、增加A的用量,化学平衡不发生移动 |
| B、当升高体系的温度时,则化学平衡正向移动,混合体系的总压必定减小 |
| C、当混合气体的密度不再变化时,则一定达到化学平衡 |
| D、当充入少量氦气时,虽总压增加,但化学平衡不发生移动 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、A为固体,改变用量不影响化学平衡;
B、反应是吸热反应升温平衡正向进行;
C、反应前后气体体积不变,质量改变,密度不变说明反应达到平衡;
D、恒容容器中加入惰气,总压增大,分压不变,平衡不动.
B、反应是吸热反应升温平衡正向进行;
C、反应前后气体体积不变,质量改变,密度不变说明反应达到平衡;
D、恒容容器中加入惰气,总压增大,分压不变,平衡不动.
解答:
解:A、A为固体,改变用量不影响化学平衡,增加A的用量,化学平衡不发生移动,故A正确;
B、反应是吸热反应升温平衡正向进行,气体物质的量减小,但混合气体总压不一定减小,故B错误;
C、反应前后气体体积不变,质量改变,密度不变说明反应达到平衡,故C正确;
D、恒容容器中加入惰气,总压增大,分压不变,平衡不动,故D正确;
故选B.
B、反应是吸热反应升温平衡正向进行,气体物质的量减小,但混合气体总压不一定减小,故B错误;
C、反应前后气体体积不变,质量改变,密度不变说明反应达到平衡,故C正确;
D、恒容容器中加入惰气,总压增大,分压不变,平衡不动,故D正确;
故选B.
点评:本题考查了化学平衡影响因素分析,平衡移动原理的分析判断是解题关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质在一定条件下可与乙烷发生化学反应的是( )
| A、氯气 | B、溴水 |
| C、氯水 | D、酸性高锰酸钾溶液 |
下列有机物的命名不正确的是( )
| A、3,3二甲基4乙基戊烷 |
| B、3,3,4三甲基己烷 |
| C、2,3,3三甲基戊烷 |
| D、2,3,3三甲基己烷 |
如图所示是短周期元素A、B、C在周期表中的位置,A、C两种元素的原子核外电子数之和等于B原子的核电荷数.下列说法正确的是( )
| A | C | |
| B |
| A、元素A和C的氢化物分子之间都存在氢键 |
| B、C原子的最外层电子数为6 |
| C、元素B只存在一种氧化物 |
| D、元素A有多种可变的化合价 |
下列说法中正确的是( )
| A、凡是放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是熵增大,非自发反应一定是熵减小或不变的反应 |
| C、自发反应在任何条件下都能实现 |
| D、自发反应在恰当的条件下才能实现 |
下列说法正确的是( )
| A、1molCO和1molN2所含分子数相等,质量相等,它们所占的体积也相等 |
| B、22.4LH2和71gCl2的物质的量相等 |
| C、非标准状况下,1mol任何气体的体积有可能是22.4L |
| D、1molHCl和1molH2O在标准状况下的体积都约是22.4L |
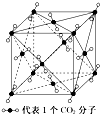 干冰晶体是一种面心立方结构,如图所示,即每8个CO2构成立 方体,且在6个面的中心又各有1个CO2分子,在每个CO2周围距离为
干冰晶体是一种面心立方结构,如图所示,即每8个CO2构成立 方体,且在6个面的中心又各有1个CO2分子,在每个CO2周围距离为
| ||
| 2 |
| A、4个 | B、8个 | C、12个 | D、6个 |
下列叙述中,正确的是( )
| A、12g碳所含的碳原子数就是阿伏加德罗常数 |
| B、氦气的摩尔质量是8g |
| C、阿伏加德罗常数通常用NA表示,6.02×1023 mol-1称为阿伏加德罗常数 |
| D、4.4g二氧化碳气体中所含的原子个数与4.2g氮气中所含的原子个数相等 |
 500℃时,将SO2和O2置于一容积固定为2L的密闭容器中发生反应,反应过程中SO2、O2和SO3物质的量变化如图所示,测得此温度下0~10min内共放出热量为a kJ.
500℃时,将SO2和O2置于一容积固定为2L的密闭容器中发生反应,反应过程中SO2、O2和SO3物质的量变化如图所示,测得此温度下0~10min内共放出热量为a kJ.