题目内容
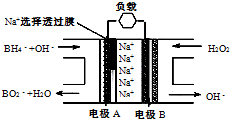 直接NaBH4/H2O2燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是( )
直接NaBH4/H2O2燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是( )| A、电极B材料中包含MnO2层,MnO2可起催化作用 |
| B、电池负极区的电极反应为:BH4-+8OH-+8e-=BO2-+6H2O |
| C、放电过程中,Na+ 从正极区向负极区迁移 |
| D、在电池反应中,每消耗1L 6 mol/LH2O2溶液,理论上流过电路中的电子为6NA个 |
考点:原电池和电解池的工作原理
专题:
分析:以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,电解质溶液呈碱性,由工作原理装置图可知,负极发生氧化反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,正极H2O2发生还原反应,得到电子被还原生成OH-,电极反应式为H2O2+2e-=2OH-,结合原电池的工作原理和解答该题.
解答:
解:A.电极B采用MnO2,为正极,H2O2发生还原反应,得到电子被还原生成OH-,MnO2既作电极材料又有催化作用,故A正确;
B.负极发生氧化反应生成BO2-,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,故B正确;
C.放电时,阳离子向正极移动,阴离子向负极移动,则Na+从负极区移向正极区,故C错误;
D.正极电极反应式为H2O2+2e-=2OH-,每消耗6molH2O2,转移的电子为12NA个,故D错误;
故选AB.
B.负极发生氧化反应生成BO2-,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,故B正确;
C.放电时,阳离子向正极移动,阴离子向负极移动,则Na+从负极区移向正极区,故C错误;
D.正极电极反应式为H2O2+2e-=2OH-,每消耗6molH2O2,转移的电子为12NA个,故D错误;
故选AB.
点评:本题考查原电池工作原理,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极以及电极方程式的书写,本题中难点和易错点为电极方程式的书写,注意化合价的变化.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
C、N、S都是重要的非金属元素.下列说法正确的是( )
| A、三者对应的氧化物均为酸性氧化物 |
| B、三者的单质直接与氧气反应都能生成两种以上氧化物 |
| C、同温度、同浓度的Na2CO3、NaNO3、Na2SO3溶液的pH:NaNO3<Na2SO3<Na2CO3 |
| D、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
下列说法错误的是( )
| A、淀粉、油脂、蛋白质都能水解,但水解产物不同 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、植物油和裂化汽油都可以使溴水褪色 |
| D、使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾 |
下列溶液在空气中加热蒸干并灼烧后,能得到相应溶质固体的是( )
| A、FeCl3 |
| B、KHCO3 |
| C、Fe2(SO4)3 |
| D、FeSO4 |
下列装置应用于实验室制氯气并回收氯化锰的实验,不能达到实验目的是( )


| A、用装置甲制取氯气 |
| B、用装置乙除去氯气中的少量氯化氢 |
| C、用装置丙分离二氧化锰和氯化锰溶液 |
| D、用装置丁蒸干氯化锰溶液不能制得MnCl2?4H2O |
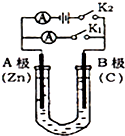 如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的溶液,按要求回答下列问题: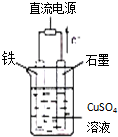 (1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气.写出负极的电极反应式
(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气.写出负极的电极反应式